Что такое синдром бланда уайта гарланда
Синдром Бланда-Уайта-Гарланда – это врожденная аномалия коронарного русла, характеризующаяся отхождением венечных артерий (чаще левой) от легочной артерии, вследствие чего значительный участок миокарда получает венозное кровоснабжение. Клинические проявления синдром Бланда-Уайта-Гарланда включают тахипноэ, утомляемость, удушье, бледность, потливость. Синдром Бланда-Уайта-Гарланда диагностируется с помощью данных аускультации, ЭКГ, УЗИ сердца, рентгенографии, аортографии, коронарографии, вентрикулографии, МРТ и КТ. Для коррекции синдрома Бланда-Уайта-Гарланда предложено несколько типов операций — реимплантация левой коронарной артерии в аорту, шунтирование артерии, перевязка устья левой венечной артерии и др.
Общие сведения
Синдром Бланда-Уайта-Гарланда (СБУГ, синдром BWG) – аномальное ответвление коронарных артерий, кровоснабжающих сердечную мышцу, от легочного ствола. В кардиологии синдром Бланда-Уайта-Гарланда составляет 0,5% от всех врожденных пороков сердца. Клинические признаки порока были изучены и описаны в 1933 г. американскими кардиологами E. Bland, P. White, J. Garland, в честь которых данная аномалия получила название «синдром Бланда-Уайта-Гарланда». Синдром Бланда-Уайта-Гарланда в 2 раза чаще наблюдается у девочек, чем у мальчиков.
Синдром Бланда-Уайта-Гарланда обычно встречается в изолированном виде, однако может сочетаться с другими пороками: дефектом межпредсердной перегородки (ДМПП), дефектом межжелудочковой перегородки (ДМЖП), тетрадой Фалло, коарктацией аорты, открытым артериальным протоком, транспозицией магистральных сосудов.

Синдром Бланда-Уайта-Гарланда
Причины
Синдром Бланда-Уайта-Гарланда формируется вследствие неправильной эмбриональной закладки венечных артерий. Предложено несколько гипотез, объясняющих эмбриогенез порока:
- отхождение коронарных сосудов начинается от легочной части артериального ствола вследствие неправильного формирования аортолегочной перегородки;
- зачаток левой венечной артерии с самого начала формируется в области легочной артерии;
- отхождение коронарной артерии формируется в области аортального и легочного клапанов. В норме в дальнейшем зачатки легочной артерии регрессируют, а развиваются только два зачатка аорты. В некоторых случаях коронарный зачаток легочной артерии сохраняется и разрастается, обусловливая аномальное отхождение коронарных сосудов от легочного ствола.
Факторы риска, предрасполагающие к развитию синдрома Бланда-Уайта-Гарланда, на сегодняшний день неизвестны; четкая связь и с какими-либо генетическими нарушениями не выявлена.
Патогенез
В норме левая коронарная артерия берет начало от левого синуса Вальсальвы, а при синдроме Бланда-Уайта-Гарланда отходит от корня легочного ствола. Ее дальнейшее ветвление, как правило, остается нормальным. Особенности внутрисердечного кровообращения при синдроме Бланда-Уайта-Гарланда, прежде всего, определяются соотношением давлений в аорте и легочной артерии.
Во внутриутробном периоде давление в легочном стволе и насыщение крови кислородом сопоставимы с аортой, поэтому аномальная левая венечная артерия обеспечивает нормальный кровоток и адекватное кровоснабжение сердечной мышцы. При рождении происходит снижение давления в легочной артерии, в результате чего часть миокарда, кровоснабжаемая аномально расположенной коронарной артерией, получает недостаточный объем слабо оксигенированной крови. Снижение коронарной перфузии сопровождается тяжелой ишемией миокарда, дисфункцией и прогрессирующим повреждением участка сердечной мышцы.
Вместе с этим, постепенно формируются межкоронарные анастомозы, обусловливающие поступление крови в аномальный сосуд не только из легочной артерии, но и из правой коронарной артерии, отходящей от аорты. По мере увеличения количества межкоронарных анастомозов направление тока крови в аномальной артерии изменяется, формируется сброс из венечного русла в легочную артерию, что приводит к развитию «феномена обкрадывания», т. е. ухудшению кровоснабжения миокарда в бассейне нормально расположенной правой коронарной артерии. Это сопровождается дальнейшим ишемическим повреждением миокарда и усугублением его дисфункции.
Характер коронарной гемодинамики может существенно изменяться при наличии сопутствующих ВПС, протекающих с легочной гипертензией (ДМПП, ДМЖП и др.). Это в известной мере затрудняет прижизненную диагностику синдрома Бланда-Уайта-Гарланда.
Таким образом, в течении синдрома Бланда-Уайта-Гарланда различают 3 патофизиологические фазы.
- Первая фаза характеризуется адекватным кровенаполнением левой венечной артерии, обусловленным высоким давлением в легочном стволе.
- Вторая фаза (критическая) обусловлена падением давления в легочной артерии и развитием анастомозов между правой и левой коронарными артериями.
- Третья фаза наступает с развитием ретроградного тока крови из левой коронарной артерии в легочный ствол и ведет к усугублению ишемии миокарда.
При аутопсии у лиц, страдавших синдромом Бланда-Уайта-Гарланда, обнаруживается увеличенное сердце шарообразной формы, резкая дилатация левого желудочка, выраженный фиброэластоз миокарда, гипертрофия и деформация папиллярных мышц, аневризмы левого желудочка, нередко — трансмуральные или субэндокардиальные инфаркты миокарда левого желудочка.
Классификация
Различают четыре анатомических варианта синдрома Бланда-Уайта-Гарланда: аномальное отхождение левой, правой, обеих или добавочной венечных артерий от ствола легочной артерии. Статистически чаще встречается неправильное ответвление левой коронарной артерии. Также принято выделять два типа синдрома, различающиеся клинической картиной:
- инфантильный (с плохо развитым коллатеральным кровоснабжением);
- взрослый (с хорошо развитым коллатеральным кровоснабжением).
Симптомы
Клинические проявления синдрома Бланда-Уайта-Гарланда, прежде всего, зависят от его варианта. Инфантильный тип обычно заявляет о себе в возрасте 2-3 месяцев. При этом отмечаются затруднения при кормлении ребенка (так называемая стенокардия кормления): учащенное храпящее дыхание, одышка, потливость, бледность кожных покровов, цианоз губ, кашель, регургитация, рвота. Приступы также могут провоцироваться дефекацией, криком, любым физическим усилием, интеркуррентными инфекциями.
Дети вялые, быстро утомляются, медленно увеличивают массу тела. Объективно определяется расширение границ сердца, глухость сердечных тонов, тахикардия, систолический шум и ритм галопа, увеличение печени, влажные хрипы в легких. Позже присоединяются отеки подкожной клетчатки, гидроторакс, асцит. Синдрома Бланда-Уайта-Гарланда является наиболее частой причиной развития инфаркта миокарда у детей. Более 90% детей с инфантильным типом погибают в течение первого года жизни от тяжелой сердечной недостаточности, нарушений ритма и проводимости сердца.
При взрослом типе синдрома межартериальные коллатерали обеспечивают достаточное коронарное кровоснабжение и относительно благоприятное развитие заболевания. Длительное время состояние больных может сохраняться стабильным. Клинические проявления могут развиваться в возрасте 3-25 лет и даже позже, характеризуясь стенокардией напряжения и стенокардией покоя, признаками сердечной недостаточности, тяжелыми аритмиями и блокадами. Иногда первым проявлением синдрома Бланда-Уайта-Гарланда служит внезапная коронарная смерть. Редким исключением является малосимптомное течение порока и его случайное выявление при плановой электрокардиографии или коронарографии в связи с инфарктом миокарда.
Диагностика
Диагностика синдрома Бланда-Уайта-Гарланда осуществляется с помощью электрокардиографии, эхокардиографии, рентгенографии грудной клетки, коронарографии, аортографии, левой вентрикулографии, зондирования полостей сердца, МРТ и МСКТ сердца.
На рентгенограммах у пациентов с синдромом Бланда-Уайта-Гарланда выявляется кардиомегалия, застой крови в легочном круге кровообращения. Характерными ЭКГ-признаками служат гипертрофия миокарда левого желудочка и его ишемическое поражение, блокада левой ножки пучка Гиса. ЭхоКГ обнаруживает систолическую дисфункцию миокарда левого желудочка с зонами гипо- и акинезии. Допплерэхокардиография нередко позволяет регистрировать турбулентный поток крови из аномальной венечной артерии в легочный ствол.
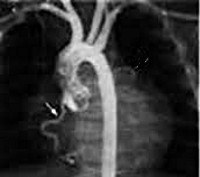
Наиболее точные сведения в отношении синдрома Бланда-Уайта-Гарланда дают аортография и селективная коронарография (КТ-коронарография, МСКТ-коронарография). При этом на ангиограммах визуализируется разветвленная правая и аномально расположенная левая коронарные артерии, ретроградный сброс контраста в легочный ствол.
В заключительной фазе развития синдрома Бланда-Уайта-Гарланда катетеризация сердца обнаруживает повышенную артериализацию крови на уровне легочного ствола, обусловленную выраженным лево-правым сбросом крови. Левая вентрикулография выявляет дилатацию полости желудочка, признаки митральной недостаточности. С помощью МРТ и МСКТ сердца определяется местоположение венечных артерий, выявляется сопутствующая патология сердца и сосудов.
Лечение синдрома Бланда-Уайта-Гарланда
Больные с синдромом Бланда-Уайта-Гарланда нуждаются в консультации кардиохирурга и тщательном обследовании с целью определения показаний и противопоказаний к оперативному лечению. Различные хирургические методы коррекции синдрома Бланда-Уайта-Гарланда направлены на обеспечение адекватного кровоснабжение миокарда в бассейне левой венечной артерии.
В случае хорошо развитого коллатерального кровообращения производится перевязка устья аномальной коронарной артерии (лигирование фистулы коронарной артерии). В этом случае всю нагрузку по кровоснабжению миокарда берет на себя нормальная правая коронарная артерия.
Другим вариантом коррекции синдрома Бланда-Уайта-Гарланда является шунтирование аномально отходящей левой коронарной артерии с помощью внутригрудных артерий (маммарокоронарное шунтирование). При синдроме Бланда-Уайта-Гарланда возможно проведение транслокации устья левой коронарной артерии в аорту, соединение левой венечной артерии и аорты с помощью тоннеля внутри легочного ствола.
Прогноз
Естественное течение синдрома Бланда-Уайта-Гарланда ассоциировано с высоким риском смерти в раннем детском (инфантильный тип) или молодом возрасте (взрослый тип). Отхождение правой коронарной артерии от ствола легочной артерии встречается крайне редко, не приводит к каким-либо клинически значимым поражениям сердца и совместимо с нормальной жизнью. Случаи отхождения обеих венечных артерий от легочного ствола прогностически неблагоприятны и приводят к гибели больных в течение первых 2-х недель жизни.
Существенно улучшается прогноз при своевременном выявлении и адекватной кардиохирургической коррекции синдрома Бланда-Уайта-Гарланда.
Источник
Синдром Бланда-Уайта-Гарланда относится к редко встречающимся врожденным аномалиям развития коронарных артерий и среди врожденных пороков выявляется только в 0,25-0,5 % случаев. При таком синдроме наблюдается неправильное ответвление венечных артерий, питающих миокард, от легочного ствола. В большинстве случаев наблюдается аномальное отхождение именно левой коронарной артерии.
Первое упоминание о синдроме Бланда-Уайта-Гарланда датировано 1886 годом и его зафиксировал Г. Брукс. Более детально данная патология была рассмотрена спустя четверть века русским патологоанатомом А.И. Абрикосовым. И только в 1933 году аномалия коронарных сосудов была подробно изучена американскими врачами Бландом, Уайтом и Гарландом. Ими были детально изучены и описаны электрокардиографические проявления и симптомы этого врожденного порока развития сосудов, и синдром был назван по их именам – BWG syndrome.
В легочной артерии течет венозная кровь. При синдроме BWG она начинает попадать в артерии, питающие миокард, а для нормального функционирования сердечной мышцы необходима обогащенная кислородом артериальная кровь. В результате миокард начинает страдать от гипоксии и не может полноценно выполнять свои функции. При таком пороке возможно возникновение опасных для жизни осложнений, таких как сердечная недостаточность, инфаркт миокарда или внезапная коронарная смерть.
По данным статистики, синдром BWG в 2 раза чаще выявляется у девочек. Как правило, эта врожденная аномалия наблюдается в изолированном виде, но в некоторых случаях может сочетаться с другими пороками развития сосудов и сердца.
В этой статье мы ознакомим вас с особенностями нарушения кровообращения при таком врожденном пороке развития сосудов, симптомами, способами выявления и лечения синдрома Бланда-Уайта-Гарланда. Эта информация поможет вам понять суть недуга, а вы сможете задать врачу возникшие у вас вопросы.
Причины
Пока ученые не смогли выяснить точных причин возникновения такой аномалии развития сосудов как синдром BWG. В отличие от других врожденных пороков сердца и сосудов, четкая взаимосвязь влияния неблагоприятных факторов на эмбрионогенез сердца при этом синдроме не была обнаружена.
Пока ученые выдвигают несколько гипотез о причине развития синдрома BWG:
- Коронарные сосуды ответвляются от легочного ствола из-за аномального формирования перегородки между аортой и легочной артерией.
- Коронарная артерия ответвляется от области легочного и аортального клапана. При нормальном развитии сосудов зачатки легочной артерии регрессируют, а продолжают развиваться только 2 зачатка будущей аорты. Под влиянием не выявленных пока факторов коронарный зачаток легочной артерии может сохраняться и продолжает расти. Так появляется аномальное ответвление венечной артерии от легочного ствола.
- Зачаток будущей венечной артерии изначально формируется в зоне легочной артерии.
Как нарушается гемодинамика и кровоснабжение миокарда
При нормальном строении сердца и сосудов левая коронарная артерия берет свое начало от левого синуса Вальсальвы, а при синдроме BWG – от корня легочного ствола. В дальнейшем она разветвляется как обычно. Такое аномальное отхождение сосуда провоцирует изменением соотношения показателей давления в легочной артерии и аорте.
Пока будущий ребенок развивается внутриутробно, оксигенация крови остается нормальной, и плод не страдает от нарушений гемодинамики. После рождения малыш начинает дышать легкими и давление в легочной артерии понижается. Такое изменение приводит к недостаточной оксигенации крови, и тот участок сердечной мышцы, который кровоснабжается аномально расположенной венечной артерией, начинает страдать от ишемии и гипоксии. Эти факторы приводят к его дисфункции, которая со временем прогрессирует и приводит к повреждению тканей миокарда.
Ребенок продолжает расти, и организм пытается компенсировать такую недостаточность кровоснабжения формированием межкоронарных анастомозов. В аномальный сосуд начинает поступать кровь не только из легочной артерии, но и из отходящей от аорты правой коронарной артерии. Количество таких анастомозов увеличивается, и в определенный момент этот факт изменяет направление тока крови в аномально развитой артерии. В результате происходит сброс из сосудов сердца в легочную артерию. Этот процесс нарушения гемодинамики получил название «феномен обкрадывания». Его название указывает на то, что в бассейне правой коронарной артерии кровоснабжение миокарда становится недостаточным, т. е. его ткани повреждаются из-за постоянной ишемии, и функциональность ухудшается.
При синдроме BWG из-за ишемии и кислородного голодания, вызывающихся нарушением кровообращения, в сердечной мышце происходят следующие изменения:
- дистрофия;
- некроз;
- разрастание рубцовой ткани;
- кальцификация;
- истончение стенки левого желудочка;
- ослабление сократительной способности.
Ответвление правой коронарной артерии при синдроме BWG наблюдается крайне редко. Оно не приводит к значительным нарушениям коронарного кровообращения и вполне совместимо с привычным образом жизни.
При ответвлении обеих коронарных артерий гемодинамика нарушается еще в большей мере, и синдром BWG приводит к смерти больного уже в первые 2 недели жизни.
 При инфантильном синдроме симптомы появляются уже в первые месяцы жизни ребенка: он становится беспокойным, часто плачет, при сосании груди у него возникает одышка
При инфантильном синдроме симптомы появляются уже в первые месяцы жизни ребенка: он становится беспокойным, часто плачет, при сосании груди у него возникает одышка
Синдром BWG может протекать в двух вариантах:
- инфантильный тип – впервые проявляется через несколько месяцев после рождения ребенка, протекает тяжело, так как межкоронарные анастомозы еще не успели сформироваться, и ткани миокарда сильнее страдают от ишемии;
- взрослый тип – впервые проявляется в возрасте от 3 до 25 (иногда более) лет, протекает более благоприятно, так как межкоронарные анастомозы уже успели сформироваться и могут компенсировать ишемию миокарда.
Инфантильный тип
Как правило, симптомы при таком варианте течения синдрома BWG впервые появляются в возрасте 2-3 месяцев. Родители могут заметить, что дыхание ребенка становится затрудненным во время кормления. Возникающая одышка напоминает клинику стенокардии – дыхание становится учащенным, храпящим, провоцирует появление пота, бледности, синюшности, срыгивания, рвоты и кашля. Ребенок может становиться беспокойным из-за боли в сердце, громко кричать, вытягивать ножки, а его пульс становится нитевидным. Такие же приступы могут возникать при натуживании во время дефекации, крике, физическом переутомлении или инфекционном заболевании (например, ОРВИ, грипп и др.). Такие дети быстро утомляются, часто бывают вялыми, подвержены инфекционным заболеваниям и медленно прибавляют в весе.
При прослушивании тонов сердца врач может определить их глухость, ритм галопа и систолический шум. Пульс у ребенка учащен, а границы сердца расширены. В легких определяются рассеянные влажные хрипы. При прощупывании живота выявляется увеличение размеров печени.
Из-за недостаточной функциональности миокарда позднее у ребенка постоянно прогрессирует сердечная недостаточность, приводящая к возникновению отеков, скоплению жидкости в плевральной и брюшной полости. На первом году жизни у больного может наступать инфаркт миокарда, а 85-90% таких маленьких пациентов погибают до года от нарушений ритма и проводимости сердца или тяжелого течения сердечной недостаточности.
Взрослый тип
При взрослом варианте синдрома BWG порок протекает более благоприятно, так как межкоронарные анастомозы уже успели развиться в достаточной мере и ткани миокарда не так сильно страдают от ишемии и кислородного голодания. До 3-25 лет больной может не знать о существовании порока из-за его бессимптомного течения.
При таком типе синдром BWG впервые проявляет себя стенокардическим приступом. Он может возникать при физической активности или в состоянии покоя. Кроме этого, у больного появляются признаки сердечной недостаточности, нарушения ритма и блокады. В некоторых случаях тяжелые аритмии могут приводить к наступлению внезапной коронарной смерти, а иногда такой летальный исход может становиться первым признаком синдрома BWG.
Диагностика
 Врач диагностирует данную патологию, используя стандартные кардиологические методы диагностики — ЭКГ, УЗИ сердца и прочие
Врач диагностирует данную патологию, используя стандартные кардиологические методы диагностики — ЭКГ, УЗИ сердца и прочие
Для выявления синдрома BWG необходимо проведение следующих видов обследования:
- ЭКГ – определяет ишемию миокарда, гипертрофию сердечной мышцы левого желудочка, вторичные блокады ножек пучка Гиса и аритмии (при взрослом типе все показатели могут оставаться в пределах нормы);
- Эхо-КГ – выявляет гипертрофию миокарда левого желудочка, систолическую дисфункцию области поражения сердечной мышцы, обратный ток крови из коронарных сосудов в легочную артерию (аномальное ответвление венечной артерии выявляется не всегда);
- рентгенография грудной клетки – определяется увеличенная тень сердца и признаки застоя крови в малом круге кровообращения;
- КТ или МСКТ-коронарография – выявляет аномальное расположение левой коронарной артерии и разветвление правой, распространение контрастного вещества по образовавшимся анастомозам и заброс контраста в легочный ствол.
Наиболее точным методом диагностики синдрома BWG является КТ- или МСКТ-коронарография. При необходимости эта методика обследования может дополняться МРТ или МСКТ сердца, которые так же позволяют выявить зону расположения коронарных артерий и сопутствующие пороки сосудов и сердца.
Лечение
Всем больным с синдромом BWG показана кардиохирургическая коррекция аномального развития сосудов. На подготовительном этапе к операции, который должен быть максимально коротким из-за высокого риска наступления смерти, больному назначается медикаментозная терапия, направленная на поддержание деятельности сердца.
Для коррекции порока могут выполняться следующие операции:
- перевязка (лигирование) аномально ответвленной коронарной артерии в месте ее отхождения от легочной артерии – выполнение такой коррекции показано только при достаточном развитии межкоронарных коллатералей;
- реимплантация в аорту устья аномальной артерии – такая коррекция проводится в большинстве случаев и заключается в соединении аорты и левой венечной артерии при помощи создания тоннеля внутри легочной артерии;
- маммокоронарное шунтирование – заключается в создании обходного пути кровоснабжения миокарда путем шунтирования левой коронарной артерии внутригрудными сосудами.
Выбор кардиохирургической методики осуществляется после всестороннего обследования пациента. При этом учитываются не только анатомические особенности синдрома BWG, но и данные о сопутствующих кардиальных и внекардиальных патологиях.
Прогнозы
При отсутствии своевременной хирургической коррекции синдрома BWG шансы на выживание ребенка невелики – около 85-90% детей погибает до года, и только 10-15% адаптируются к пороку и взрослеют дальше. В некоторых случаях наступает внезапная коронарная смерть. Такой летальный исход возможен как при инфантильном, так и при взрослом типе синдрома BWG.
При своевременной и адекватной кардиохирургической помощи прогнозы на выживание больного улучшаются. Однако даже после выполнения операции риск возникновения осложнений или наступления летального исхода остается высоким.
Синдром Бланда-Уайта-Гарланда является редким, но крайне опасным врожденным пороком развития сосудов, который сопровождается ненормальным ответвлением венечных артерий. Заподозрить наличие такой патологии возможно по появлению стенокардических приступов и наличию шумов в сердце. Подтвердить этот диагноз при помощи традиционных методик обследования достаточно сложно, и для выявления аномалий сосудов необходимо выполнение КТ- или МСКТ-коронарографии. При обнаружении признаков синдрома больному назначается кардиохирургическое лечение, которое не должно откладываться из-за высокого риска развития тяжелых осложнений и наступления внезапной коронарной смерти. Иногда такая аномалия развития сосудов впервые манифестирует внезапным наступлением летального исхода до года жизни или в молодом возрасте.
Источник
