Что такое юношеский гипоталамический синдром

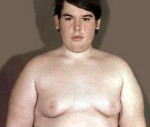
Гипоталамический синдром – комплекс эндокринных, обменных, вегетативных расстройств, обусловленных патологией гипоталамуса. Характеризуется изменением (чаще увеличением) массы тела, головными болями, неустойчивостью настроения, гипертензией, нарушением менструального цикла, повышенным аппетитом и жаждой, усилением или снижением либидо. Для диагностики гипоталамического синдрома проводится расширенное гормональное исследование, ЭЭГ, МРТ головного мозга, при необходимости УЗИ щитовидной железы, надпочечников. Лечение гипоталамического синдрома заключается в подборе эффективной стимулирующей или ингибирующей гормональной терапии, проведении симптоматического лечения.
Общие сведения
Гипоталамический синдром – комплекс эндокринных, обменных, вегетативных расстройств, обусловленных патологией гипоталамуса. Характеризуется изменением (чаще увеличением) массы тела, головными болями, неустойчивостью настроения, гипертензией, нарушением менструального цикла, повышенным аппетитом и жаждой, усилением или снижением либидо. Прогноз зависит от тяжести поражения гипоталамуса: от возможности полного выздоровления до прогрессирования заболевания (развитие выраженного ожирения, стойкой гипертонии, бесплодия и т. д.).
Патология гипоталамической области часто встречается в эндокринологической, гинекологической, неврологической практике, вызывая сложности в диагностике из-за многообразия форм проявления. Гипоталамический синдром чаще развивается в подростковом (13-15 лет) и репродуктивном (31-40 лет) возрасте, преобладая у лиц женского пола (12,5–17,5% женщин).
Проблема медицинской и социальной значимости гипоталамического синдрома определяется молодым возрастом пациентов, быстро прогрессирующим течением заболевания, выраженными нейроэндокринными нарушениями, нередко сопровождающимися частичным снижением или полной утратой трудоспособности. Гипоталамический синдром вызывает серьезные нарушения репродуктивного здоровья женщины, вызывая развитие эндокринного бесплодия, поликистоза яичников, акушерские и перинатальные осложнения.
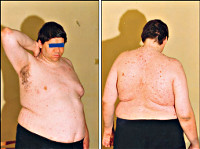
Гипоталамический синдром
Причины развития гипоталамического синдрома
Гипоталамический отдел головного мозга отвечает за регуляцию гуморальных и нервных функций, обеспечивающих гомеостаз (стабильность внутренней среды). Гипоталамус выполняет роль высшего вегетативного центра, регулирующего обмен веществ, терморегуляцию, деятельность кровеносных сосудов и внутренних органов, пищевое, половое поведение, психические функции. Кроме того, гипоталамус управляет физиологическими реакциями, поэтому при его патологии нарушается периодичность тех или иных функций, что выражается вегетативным кризом (пароксизмом).
Вызывать нарушения деятельности гипоталамуса и развитие гипоталамического синдрома могут следующие причины:
- опухоли головного мозга, сдавливающие гипоталамическую область;
- черепно-мозговые травмы с прямым повреждением гипоталамуса;
- нейроинтоксикации (токсикомания, наркомания, алкоголизм, производственные вредности, экологическое неблагополучие и т. д.);
- сосудистые заболевания, инсульт, остеохондроз шейного отдела позвоночника;
- вирусные и бактериальные нейроинфекции (грипп, ревматизм, малярия, хронический тонзиллит и др.);
- психогенные факторы (стрессы, шоковые ситуации, умственные нагрузки);
- беременность и сопряженные с ней гормональные перестройки;
- хронические заболевания с вегетативными компонентами (бронхиальная астма, гипертония, язвы желудка и двенадцатиперстной кишки, ожирение);
- конституциональная недостаточность гипоталамической области.
Классификация гипоталамического синдрома
Клиническая эндокринология насчитывает большое число исследований по изучению гипоталамического синдрома. Результаты этих исследований легли в основу современной расширенной классификации синдрома.
По этиологическому принципу гипоталамический синдром подразделяется на первичный (вследствие нейроинфекций и травм), вторичный (вследствие конституционального ожирения) и смешанный.
По ведущим клиническим проявлениям выделяют следующие формы гипоталамического синдрома:
- вегетативно-сосудистую;
- нарушения терморегуляции;
- гипоталамическую (диэнцефальную) эпилепсию;
- нейротрофическую;
- нервно-мышечную;
- псевдоневрастеническую и психопатологическую;
- расстройство мотиваций и влечений;
- нейроэндокринно-обменные расстройства.
Выделяют клинические варианты гипоталамического синдрома с преобладанием конституционального ожирения, гиперкортицизма, нейроциркуляторных нарушений, герминативных расстройств.
Тяжесть проявления гипоталамического синдрома может быть легкой, средней и тяжелой формы, а характер развития – прогрессирующий, стабильный, регрессирующий и рецидивирующий. В пубертатном периоде гипоталамический синдром может протекать с задержкой или ускорением полового созревания.
Симптомы гипоталамического синдрома
Проявления гипоталамического синдрома зависят от зоны поражения гипоталамуса (передний или задний отделы) и вызванных нейрогуморальных расстройств в гипоталамо-гипофизарной области. В проявлениях гипоталамического синдрома чаще преобладают следующие нарушения:
- вегетативно-сосудистые – 32%,
- эндокринно-обменные – 27%,
- нервно-мышечные – 10%,
- нарушения терморегуляции и др. — 4% и т. д.
Гипоталамический синдром проявляется общей слабостью, повышенной утомляемостью, физическим и психическим истощением, плохой переносимостью смены метеорологических условий, покалываниями в сердце, склонностью к аллергическим реакциям, неустойчивым стулом, чувством нехватки воздуха, эмоциональными расстройствами (тревогой, приступами панического страха), нарушениями сна, повышенной потливостью. Объективно выявляются тахикардия, асимметрия артериального давления со склонностью к его повышению, тремор пальцев и век.
У большей части пациентов гипоталамический синдром протекает пароксизмально (приступообразно), чаще в виде вагоинсулярных и симпатико-адреналовых кризов. Вазоинсулярные кризы при гипоталамическом синдроме сопровождаются чувством жара, прилива к лицу и голове, головокружением, удушьем, неприятными ощущениями в эпигастрии, тошнотой, замиранием сердца, потливостью, общей слабостью. Может наблюдаться усиленная перистальтика кишечника с послаблением стула, учащенное и обильное мочеиспускание, повторные позывы в туалет. Возможно развитие аллергических проявлений в форме крапивницы и даже отека Квинке. Частота сердечных сокращений урежается до 45-50 уд. в мин., АД снижается до 90/60-80/50 мм рт. ст.
Симпатико-адреналовые кризы при гипоталамическом синдроме могут провоцироваться эмоциональным напряжением, изменением метеоусловий, менструацией, болевыми факторами и др. Пароксизмы обычно возникают внезапно вечером или ночью, иногда им предшествуют предвестники: головная боль, изменение настроения, покалывание в области сердца, вялость. Во время приступа появляется озноб, тремор, «гусиная кожа», сердцебиение, похолодание и онемение конечностей, подъем АД до 150/100-180/110 мм рт. ст., тахикардия до 100-140 уд. в мин. Иногда симпатико-адреналовые кризы сопровождаются повышением температуры до 38-39°С, возбуждением, беспокойством, страхом смерти (паническими атаками).
Продолжительность криза может быть от 15 мин. до 3 и более часов, после чего на протяжении нескольких часов сохраняется слабость и страх повторения подобного приступа. Часто при гипоталамическом синдроме кризы носят смешанный характер, сочетая симптомы вагоинсулярного и симпатико-адреналового кризов.
Нарушение терморегуляции при гипоталамическом синдроме сопровождается развитием гипертермического криза, характеризующегося внезапным скачком температуры тела до 39-40 °С на фоне длительного субфебрилита. Для терморегуляционных нарушений типично утреннее повышение температуры и ее снижение к вечеру, отсутствие эффекта от приема жаропонижающих препаратов. Расстройства терморегуляции чаще наблюдаются в детском и юношеском возрасте и зависят от физического и эмоционального напряжения. У подростков они нередко связаны со школьными занятиями и исчезают в каникулярный период.
Проявлениями терморегуляционных нарушений при гипоталамическом синдроме могут служить постоянная зябкость, непереносимость сквозняков и низких температур. Такие пациенты постоянно кутаются, носят одежду не по погоде, даже в теплое время не открывают форточки и окна, избегают принимать ванну. Расстройство мотиваций и влечений при гипоталамическом синдроме характеризуется эмоционально-личностными нарушениями, различными фобиями, изменением либидо, патологической сонливостью (гиперсомнией) или бессонницей, частой сменой настроения, раздражительностью, гневом, слезливостью и т. д.
Нейроэндокринно-обменные расстройства при гипоталамическом синдроме проявляются нарушением белкового, углеводного, жирового, водно-солевого обмена, булимией, анорексией, жаждой. Нейроэндокринные нарушения могут сопровождаться синдромами Иценко-Кушинга, несахарного диабета с полиурией, полидипсией и низкой относительной плотностью мочи, акромегалией, ранним климаксом у молодых женщин, изменениями в щитовидной железе. Могут наблюдаться дистрофия костей и мышц, нарушения трофики кожи (сухость, зуд, пролежни), изъязвления слизистых внутренних органов (пищевода, 12-перстной кишки, желудка). Для гипоталамического синдрома характерно хроническое или длительное течение с рецидивами и обострениями.
Осложнения гипоталамического синдрома
Диагностика гипоталамического синдрома
Полиморфная клиника гипоталамического синдрома представляет немалые трудности в его диагностике. Поэтому ведущими критериями диагностики гипоталамического синдрома служат данные специфических тестов: сахарной кривой, термометрии в трех точках, ЭЭГ головного мозга, трехдневной пробы Зимницкого.
Глюкозу крови при гипоталамическом синдроме исследуют натощак и с нагрузкой 100 г сахара, определяя уровень глюкозы через каждые 30 минут. При гипоталамическом синдроме встречаются следующие варианты сахарной кривой:
- гипергликемический (подъем уровня глюкозы выше нормы);
- гипогликемический (содержание глюкозы ниже нормы);
- двугорбовый (снижение уровня глюкозы чередуется с новым подъемом);
- торпидный (небольшой подъем глюкозы фиксируется в одной точке).
Термометрию при гипоталамическом синдроме проводят в трех точках: обеих подмышечных впадинах и в прямой кишке. Термометрические нарушения могут выражаться в изотермии (равной температуре в прямой кишке и подмышечных областях, при норме в прямой кишке на 0,5-1°С выше); гипо- и гипертермии (в подмышечных впадинах температура ниже или выше нормы); термоинверсии (температура в прямой кишке ниже, чем в подмышечных впадинах).
Электроэнцефалография выявляет изменения, затрагивающие глубинные структуры мозга. В трехдневной пробе по Зимницкому у пациентов с гипоталамическим синдромом изменяется соотношение выпитой и выделяемой жидкости, ночного и дневного диуреза. Методом МРТ головного мозга при гипоталамическом синдроме выявляется повышенное внутричерепное давление, последствия гипоксии и травм, опухолевые образования.
Обязательным критерием диагностики гипоталамического синдрома является определение гормонов (пролактина, ЛГ, эстрадиола, ФСГ, тестостерона, кортизола, ТТГ, Т4 (свободного тироксина), адренотропного гормона в крови и 17-кетостероидов в суточной моче) и биохимических показателей для выявления эндокринно-обменных нарушений. Дифференцировать гипоталамический синдром с органическим поражением других систем позволяет УЗИ надпочечников, УЗИ щитовидной железы и внутренних органов. При необходимости дополнительно проводится МРТ или КТ надпочечников.
Лечение гипоталамического синдрома
Комплекс мероприятий по лечению гипоталамического синдрома должен осуществляться совместными усилиями эндокринолога, невролога и гинеколога (у женщин). Подбор методов лечения гипоталамического синдрома всегда индивидуален и зависит от ведущих проявлений. Целью терапии гипоталамического синдрома является коррекция нарушений и нормализация функции гипоталамических структур головного мозга.
На первом этапе лечения проводят устранение этиологического фактора: санацию инфекционных очагов, лечение травм и опухолей и т. д. При интоксикациях алкоголем, наркотиками, инсектицидами, пестицидами, тяжелыми металлами проводится активная дезинтоксикационная терапия: внутривенно вводятся солевые растворы, тиосульфат натрия, глюкоза, физиологический раствор и др. Для профилактики симпатико-адреналовых кризов назначаются пирроксан, алкалоиды красавки + фенобарбитал, сульпирид, тофизопам, антидепрессанты (тианептин, амитриптилин, миансерин и др.).
Нейроэндокринные нарушения корректируются заместительными, стимулирующими или тормозящими гормональными препаратами, назначением диеты и регуляторов нейромедиаторного обмена (бромокриптин, фенитоин) курсом до полугода. При развитии посттравматического гипоталамического синдрома проводят дегидратирующую терапию, цереброспинальную пункцию. При нарушениях обмена назначается диетотерапия, анорексанты, витамины.
При гипоталамическом синдроме назначаются средства, улучшающие мозговое кровообращение (пирацетам, гидрализат головного мозга свиней, винпоцетин), витамины группы В, аминокислоты (глицин), препараты кальция. В лечение гипоталамического синдрома включают рефлексотерапию, физиопроцедуры, лечебную гимнастику. В структуре лечения гипоталамического синдрома важная роль отводится нормализации режима отдыха и работы, диете, нормализации массы тела, курортотерапии.
Прогноз и профилактика гипоталамического синдрома
Гипоталамический синдром может приводить к снижению и утрате работоспособности в случаях часто повторяющихся вегетативных пароксизмов. Таким пациентам с учетом их профессиональной деятельности может устанавливаться инвалидность III группы. Резко выраженные нейроэндокринно-обменные формы гипоталамического синдрома также могут приводить к потере трудоспособности с установлением III или II группы инвалидности.
Поскольку кризы при гипоталамическом синдроме, как правило, возникают в определенное время и при изменениях метеоусловий, значительных эмоциональных и физических перенапряжениях, их профилактика заключается в предупреждающем приеме седативных средств, антидепрессантов, транквилизаторов. Также, по возможности, необходимо исключить провоцирующие приступы факторы, нервно-психические и физические нагрузки, работу в ночные смены.
Источник
 В последнее время распространенность гипоталамического синдрома пубертатного периода (ГСПП) выросла вдвое. Проблема медицинской и социальной значимости гипоталамичного синдрома (ГС) определяется молодым возрастом пациентов, быстро прогрессирующим течением заболевания, выраженными нейроэндокринными нарушениями, которые довольно часто сопровождаются пониженной или полной потерей работоспособности. ГС вызывает серьезные нарушения репродуктивного здоровья девочек, становится причиной развития эндокринного бесплодия, поликистоза яичников, акушерских и перинатальных осложнений в будущем.
В последнее время распространенность гипоталамического синдрома пубертатного периода (ГСПП) выросла вдвое. Проблема медицинской и социальной значимости гипоталамичного синдрома (ГС) определяется молодым возрастом пациентов, быстро прогрессирующим течением заболевания, выраженными нейроэндокринными нарушениями, которые довольно часто сопровождаются пониженной или полной потерей работоспособности. ГС вызывает серьезные нарушения репродуктивного здоровья девочек, становится причиной развития эндокринного бесплодия, поликистоза яичников, акушерских и перинатальных осложнений в будущем.
Гипоталамо-гипофизарный нейросекреторный комплекс (ГГНСК) является высшим регулятором организма, который координирует эндокринную регуляцию обмена веществ с работой вегетативной нервной системы и эмоционально-поведенческими реакциями. Нарушение взаимодействия отдельных отделов ГГНСК приводит к развитию гипоталамического синдрома у детей и подростков, а нарушение регуляторной функции ГГНСК приводит к активации глюкокортикоидной функции коры надпочечников и сопровождается нарушениями жирового и углеводного обмена.
В гипоталамо-гипофизарный комплекс входят:
- гипоталамус — отдел промежуточного мозга и центральная цепь лимбической системы;
- нейрогипофиз — состоит из двух частей; передняя часть — срединное возвышение и задняя — собственно задняя доля гипофиза
- аденогипофиз — передняя доля гипофиза.
При патологии гипоталамической области возникает симптомокомплекс, который характеризуются вегетативными, эндокринными, обменными и трофическими расстройствами и который зависит от локализации поражения гипоталамуса (в заднем или переднем отделе).
Гипоталамус является частью головного мозга, где происходит интеграция нервных и гуморальных функций, что обеспечивает неизменность, стабильность внутренней среды — гомеостаза. Гипоталамус выполняет роль высшего вегетативного центра, регулирует обмен веществ, терморегуляцию, деятельность кровеносных сосудов и внутренних органов, пищевое и половое поведение, психологические функции. Кроме того, гипоталамус управляет физиологическими реакциями, поэтому его патология может нарушать определенную функцию и проявляться кризом вегетативного характера.
Гипоталамический синдром пубертатного периода — нейроэндокринный синдром возрастной перестройки организма с дисфункцией гипоталамуса, гипофиза и других эндокринных желез. Синонимы: ожирение с розовыми растяжками; синдром Симпсона — Пейджа; пубертатный базофилизм; базофилизм полового созревания; юношеский гиперкортицизм; пубертатный гиперкортизолизм; юношеский кушингоид; функциональный кушингоид; пубертатно-юношеский диспитуитаризм; транзиторный ювенильный диэнцефальный синдром, юношеский гипоталамический синдром пубертатного периода; гипоталамический синдром периода полового созревания; диэнцефальная гиперандрогения (шифр по МКБ-10 — Е.33.0).
Это наиболее распространенная эндокринно-обменная патология подростков, частота которой в последние годы значительно увеличилась. ГСПП чаще начинается на фоне полового созревания в возрасте 10-18 лет (средний возраст — 16-17 лет). Общепринято, что мальчики болеют чаще, чем девочки.
Гипоталамический синдром пубертатного периода — нейроэндокринный синдром, возникающий в пубертатном или постпубертатном периоде вследствие функциональных эндокринных нарушений. В основном сложно выяснить его главную причину, поскольку клинические проявления в манифестной форме часто наступают спустя годы после воздействия причинного фактора.
ГСПП — заболевание, при котором, как правило, формируется вторичное, то есть не связанное с недостаточностью лептина, ожирение. Однако ГСПП может развиваться первично (у подростков с нормальной массой тела) и вторично (у подростков с первичным лептинзависимым ожирением). Факторы риска развития первичного ГСПП:
- патологическое течение беременности у матери больного (фетоплацентарная недостаточность, токсикозы или гестозы I и II половины беременности)
- осложненное течение беременности (острые болезни и обострение хронических болезней матери во время беременности, отравления, интоксикации и т.д.);
- патологические или осложненные роды (преждевременные роды, слабость родовой деятельности, обвитие пуповиной и т.д.);
- родовые травмы (асфиксия, черепно-мозговые травмы)
- перинатальная энцефалопатия
- опухоли головного мозга, которые сдавливают гипоталамическую область;
- нейротоксикоз у детей раннего возраста;
- черепно-мозговые травмы в детском возрасте (прямые поражения гипоталамуса)
- нейроинфекции (менингоэнцефалиты, арахноидиты и васкулиты) у детей
- нейроинтоксикации (наркомания, алкоголизм, производственные вредности, экологическое неблагополучие)
- неэндокринные аутоиммунные заболевания;
- рецидивирующие бронхиты, острые респираторные вирусные инфекции, хронические очаги инфекции носоглотки и придаточных пазух носа, частые ангины;
- острые вирусные заболевания (корь, паротит, грипп, гепатит)
- хронические заболевания с вегетативным компонентом (бронхиальная астма, гипертензия, язва желудка и двенадцатиперстной кишки, ожирение);
- хронический стресс, эндогенные депрессии, умственные перегрузки;
- аутоаллергические заболевания центральной нервной системы;
- злоупотребление анаболическими стероидами;
- употребление гормональных контрацептивов девочками-подростками; беременность и аборты в подростковом возрасте.
Вторичный ГСПП развивается на фоне лептинового (алиментарно-конституционального, гиподинамического ожирения). Заболевание характеризуется дисфункцией гипоталамуса с нарушением продукции аденогипофизотропных гормонов (кортиколиберина, соматолиберина) и, как следствие, дисфункцией аденогипофиза — диспитуитаризмом с нарушением секреции тропных гормонов: адренокортикотропного, соматотропного, лютеинизирующего.
Характерными являются: соматотропная гиперфункция аденогипофиза с повышенной продукцией соматолиберина и, как следствие, усиление роста; нарушение продукции гонадолиберина и гонадотропинов, что приводит к раннему или наоборот, позднему половому созреванию; гиперфункция базофильных клеток аденогипофиза без их гиперплазии и функциоональный гиперкортицизм. Нарушается синтез дофамина, серотонина, эндорфинов, развивается гиперпролактинемия, что проявляется развитием гинекомастии (чаще ложной, вследствие гиноидного ожирения).
Наблюдается гиперфункция гипоталамо-гипофизарно-тиреоидно-надпочечниковой системы с гиперпродукцией кортиколиберина, кортикотропина, глюкокортикоидов и андрогенов надпочечников, нарушением продукции тиреолиберина, тиреотропного гормона и гормонов щитовидной железы. Признаком ГСПП у подростков является преимущественно гиперпродукция кортизола и дегидроэпиандростерона .
Механизм ожирения при гипоталамическом синдроме пубертатного периода связан с собственно липогенетическим эффектом адренокортикотропного гормона и глюкокортикоидов (превращение углеводов в жирные кислоты) и действием кортикотропина на бета-клетки островков Лангерганса с выделением инсулина
Также можно выделить наследственные факторы риска ГС, особенно те, которые имеют аутосомно-доминантный тип наследования: гипертоническая болезнь, ожирение, сахарный диабет 2-го типа, аутоиммунные эндокринные синдромы и болезни. Риск развития ГС значительно возрастает, если есть три и более фактора риска одновременно.
Гипоталамический синдром — сочетание вегетативных, эндокринных, обменных и трофических расстройств, обусловленных поражением гипоталамуса. Непременным компонентом ГС являются нейроэндокринные расстройства.
Период манифестации ГСПП в раннем пубертате обусловлен активацией тропных функций гипофиза, прежде всего адренокортикотропной, гонадотропной, соматотропной, тиреотропной, что вызывает пубертатный «скачок» роста и проявляется изменениями функционирования надпочечников, гонад, щитовидной железы. Преимущественно при ГСПП нарушаются физиологические обратные связи и секреция гормонов, особенно надпочечников.
В этот период значительно возрастает нагрузка на гипоталамо-гипофизарную систему, что приводит к возникновению её дисфункции при действии патогенных факторов. Главным звеном патогенеза является нарушение синтеза и метаболизма моноаминов (особенно нейропептидов, серотонина, норадреналина), что приводит к гиперактивации тропных функций гипофиза, прежде всего кортикотропной и гонадотропной, в меньшей степени соматотропной и тиреотропной функций. Формируется дисфункциональная обратная связь между центральными и периферическими эндокринными железами, развиваются гормонально-обменные нарушения.
Повышение секреции гонадотропинов приводит к стимуляции гонад и повышению уровня общего и свободного тестостерона (гипертестостеронемия) у мальчиков 10-14-летнего возраста и прогестерона (гиперпрогестеронемия) у девочек аналогичного возраста.
При ГСПП наблюдается активация гипофизарно-тиреоидной системы, что сопровождается умеренным повышением уровня тиреотропного гормона. В дальнейшем это приводит к стимуляции щитовидной железы, которая увеличивается в объеме с одновременным увеличением секреции тиреоидных гормонов, преимущественно трийодтиронина. Секреция пролактина остается нормальной в течение заболевания.
Манифестация ГС отмечается на фоне активации симпатоадреналовой системы (САС), повышения секреции серотонина и снижения уровня мелатонина.
С прогрессированием патологии резервы САС уменьшаются, однако секреция серотонина остается повышенной. Показатели уровня мелатонина теснее связаны с клиническими проявлениями ГС и при рецидивирующем неблагоприятном течении патологии остаются низкими.
Значительную роль в патогенезе ГСПП играет гормон жировой ткани лептин, отвечающий за усиление чувства насыщения. Концентрация лептина в крови больных ГС во много раз превышает физиологические показатели, особенно при абдоминальном типе ожирения. На этом фоне формируется лептинорезистентность.
На фоне вышеупомянутых гормональных нарушений возникает инсулинорезистентность (ИР), что приводит к повышению секреции иммунореактивного инсулина и С-пептида. Уровень гиперинсулинемии и ИР напрямую зависит от степени ожирения и значительно возрастает при абдоминальном его типе.
Ведущее патогенетическое значение имеет дизрегуляция жирового (рост содержания лептина в крови сопровождается повышением аппетита, что указывает на нарушение обратных связей регуляции пищевого поведения) и углеводного обменов (гиперинсулинемия приводит к быстрому наращиванию жировой и белковой массы тела и развитию артериальной гипертензии).
Считается, что гиперинсулинемия вызывает зазадержку натрия и воды и влияет на дистальные отделы нефрона, дозозависимо стимулирует симпатическую нервную систему, увеличивает содержание катехоламинов в крови. Развитие ГСПП сопровождается повышением активности протеолитических ферментов — коллагеназы и эластазы, нарушением обмена белков соединительной ткани.
К основным метаболическим нарушениям при ГСПП относятся нарушения липидного обмена. Наиболее характерным для больных ГСПП является IV тип дислипопротеинемии:
- повышение концентрации триглицеридов (ТГ);
- повышение уровня холестерина (ХС) липопротеинов очень низкой плотности (ЛПОНП)
- нормальный уровень общего холестерина (ОХС)
- повышение уровня липопротеинов очень низкой плотности и низкой плотности (ЛПНП).
Реже возникает дислипопротеинемия II-А типа, когда повышаются уровни ЛПНП с умеренным увеличением ОХС при сохранении нормальных показателей ТГ.
На фоне ИР и гиперинсулинемии при ГС возникает нарушение углеводного обмена. У больных ГСПП возникают характерные нарушения обмена белков соединительной ткани. Почти у трети больных определяется «плоская» (гиперинсулинемическая) гликемическая кривая. Часто диагностируется нарушение толерантности к углеводам, особенно при типичном клиническом варианте ГС, и именно у этих больных показатели индекса инсулинорезистентности НОМА-ИR (homeostasis model assessment) достигают максимальных значений, хотя и при других вариантах заболевания значительно превышают нормативные.
Острая стадия заболевания характеризуется повышением функциональной активности центральных отделов САС и сопровождается повышением секреции катехоламинов и серотонина, что возбуждает ядра гипоталамуса, ответственные за репродуктивную функцию. Чрезмерная активация гипоталамо-гипофизарно-надпочечниковой системы происходит за счет повышения уровня тропных гормонов гипофиза.
Гормональный дисбаланс приводит к эндокринно-обменным нарушениям: жирового, углеводного и водно-электролитного обмена, к которым присоединяется вторичная дисфункция эндокринных желез. Через два-три года наблюдается истощение катехоламин- и серотонинпродуцирующих структур. Снижается активность гипоталамуса, гипофиза и зависимых от них эндокринных желез, что приводит к снижению уровня секреции соответствующих гормонов. При этом сохраняется гиперинсулинизм. Заболевание переходит в хроническую стадию, которая продолжается не менее четырех лет — на первый план выходят нейровегетативные симптомы.
Главным патогенетическим и клиническим аспектом ГСПП является артериальная гипертензия (АГ). Механизмы, обусловливающие взаимосвязь между АГ и ожирением, сложные и многофакторные. Так, ожирение при ГСПП ассоциировано с эндотелиальной дисфункцией, дислипидемией, избыточным образованием С-реактивного протеина, повышенной вязкостью крови, нарушением толерантности к глюкозе, микроальбуминурией, повышением уровня маркеров воспаления, ремоделированием сосудов, гипертрофией миокарда левого желудочка и преждевременным атеросклерозом — практически со всеми факторами риска развития сердечно-сосудистых заболеваний и поражения органов-мишеней при АГ. Все эти факторы играют важную роль в повышении артериального давления (АД) и развитии АГ у детей и подростков с ГСПП.
В то же время в патогенезе ГСПП одно из ведущих мест принадлежит гиперинсулинемии и ИР, способствующих активации оксидативного стресса, гипоксии тканей, гиперпродукции инсулиноподобного фактора роста на фоне нарушений углеводного, липидного, белкового обмена, гемодинамических и других свойств крови. Гиперинсулинемия активирует рецепторы АТ-I, АТ-II, способствует развитию АГ и атеросклероза, активирует САС, повышает уровень эндотелина-1. АГ тесно связана с высоким уровнем ренина плазмы, плазминогеном, инсулиноподобным фактором роста, которые играют важную роль в развитии ГСПП.
Развитие АГ при ГСПП в значительной степени связано с увеличением потребности организма в кислороде, которая возникает при избыточной массе тела. Ожирение сопровождается компенсаторным повышением сердечного выброса за счет роста ударного объема и объема циркулирующей крови. При этом общее периферическое сосудистое сопротивление снижается незначительно и неадекватно, в результате чего повышается АД. В свою очередь, гиперволемический и и гиперкинетический типы кровообращения приводят к повышению нагрузки на сердце, что создает замкнутый «порочный круг».
Гиперактивность САС имеет решающее значение в развитии сопутствующих метаболических нарушений, таких как инсулинорезистентность (ИР) и гиперлипидемия. Активация симпатической нервной системы (СНС) при ГСПП является одним из патогенетических механизмов цепи переедания: гиперинсулинемия — ИР — повышение продуктов метаболизма жирных кислот. СНС способствует развитию периферической ИР, тогда как гиперинсулинемия осуществляет рестимулирующее действие на СНС, замыкая этим «патологический круг».
Источник
