Что такое инсулиновый аутоиммунный синдром с гипогликемией
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 26 февраля 2013;
проверки требуют 7 правок.
Гипогликеми́ческий синдро́м — клинический симптомокомплекс, развивающийся вследствие дисбаланса в системе регуляции уровня глюкозы в плазме крови, приводящий к гипогликемической реакции организма. Гипогликемией принято считать снижение плазменной концентрации глюкозы до уровня ниже 2,2—2,8 ммоль/л. Наиболее часто гипогликемии развиваются в процессе лечения сахарного диабета (см. Гипогликемическая кома), однако эти состояния не включены в понятие гликемический синдром[1].
Этиология и патогенез[править | править код]
Патогенетической основой гипогликемии является повышенный клиренс глюкозы и/или снижение поступления глюкозы в кровь. Избыточный клиренс глюкозы наиболее часто развивается при гиперинсулинизме, который подразделяется на эндогенный и экзогенный[1]:
- причиной эндогенного гиперинсулинизма, приводящего к гликемическому синдрому, могут быть автономная секреция инсулина, а также рассогласование процессов поступления глюкозы из кишечника с секреторной реакцией β-клеток, которое, в свою очередь, может быть связано с нарушением пропульсивной и/или эндокринной функции ЖКТ, а в крайне редких случаях — с обратимым связыванием инсулина антителами (болезнь Хирата);
- причиной экзогенного гиперинсулинизма является введение инсулина или стимуляторов его секреции. Повышенный клиренс глюкозы ведёт к гипогликемии только при неадекватной продукции глюкозы печенью, которая может быть обусловлена печёночной недостаточностью, нарушением гликогенолиза в результате ферментативных дефектов (гликогенозы) или его вторичного подавления при непереносимости фруктозы, нарушением глюконеогенеза в результате недостаточности стимулирующих его гормонов, прежде всего глюкокортикоидов (надпочечниковая недостаточность), или его подавления алкоголем.
Избыточный клиренс глюкозы из плазмы крови наблюдается при её активном поглощении крупными опухолями:
- печени (синдром Вольфа-Надлера-Элиота),
- коры надпочечника (синдром Андерсона) мезенхимального происхождения (синдром Деже-Петтера), которые, кроме того, могут секретировать инсулиноподобные субстанции.
Снижение поступления глюкозы в плазму крови происходит при синдроме мальабсорбции, длительном голодании. При тяжёлой органной недостаточности большинство этапов углеводного обмена нарушены одновременно.
Классификация[править | править код]
Клиническая классификация гипогликемического синдрома[1]:
I. Тощаковая (голодовая) гипогликемия.
- А. Эндогенный гиперинсулинизм:
- инсулинома;
- гиперплазия инсулярного аппарата поджелудочной железы;
- эктопическая секреция инсулина и/или инсулиноподобных факторов.
- Б. Токсическая и артифициальная гипогликемия после введения:
- инсулина, сульфаниламидов (СА-препаратов), алкоголя;
- пентамидина, хинина, салицилатов и других.
- В. Тяжёлая органная недостаточность (печёночная, сердечная и сепсис).
- Г. Не β-клеточные опухоли (печени, коры надпочечника, мезенхимомы).
- Е. Гипогликемия у детей: неонатальная, гликогенозы, кетогенная гипогликемия.
II. Постпрандиальная (реактивная) гипогликемия.
- А. Постпрандиальный гипогликемический синдром: при нарушении пассажа пищи по ЖКТ, идиопатический.
- Б. Дефекты ферментов углеводного метаболизма, галактоземия, непереносимость фруктозы.
- В. Аутоиммунный инсулиновый синдром (болезнь Хирата).
Клиническая картина[править | править код]
Характеризуется сочетанием нейроглюкопенических и адренергических симптомов[1].
Диагностика[править | править код]
При заболеваниях, сопровождающихся гипогликемическим синдромом, диагностических проблем обычно не возникает, поскольку в их клинической картине гипогликемический синдром отходит на второй план. Диагноз верифицируется наличием гипогликемической симптоматики, лабораторно зарегистрированной гипогликемии, которая легко купируется введением глюкозы (триада Уиппла)[1].
Дифференциальная диагностика[править | править код]
Принципиально разделение голодовой и постпрандиальной (через 2—4 часа после еды) формы гипогликемического синдрома[1]:
- голодовая форма, в большинстве случаев, обусловлена органической патологией (инсулинома, гиперплазия инсулярного аппарата поджелудочной железы). В случае выявления голодовой гипогликемии, а также во всех сомнительных случаях пациенту показано проведение пробы с трёхдневным (72-часовым) голоданием для исключения инсулиномы;
- постпрандиальная форма гипогликемического синдрома встречается при многих состояниях, ведущей патогенетической особенностью которых является рассогласование процессов поступления глюкозы из просвета кишечника с действием факторов, регулирующих её уровень в плазме крови.
При экзогенном введении инсулина (артифициальный гипогликемический синдром) его высокий плазменный уровень будет сочетаться с отсутствием или неадекватно низким уровнем C-пептида.
Токсический гипогликемический синдром возможен на фоне передозировки сульфаниламидных препаратов, пентамидина, салицилатов, анаприлина, хинидина, галоперидола (особенно в сочетании с приёмом алкоголя), метаболиты которых могут быть определены в моче и крови.
Наибольшие затруднения вызывает диагностика постпрандиальной формы гипогликемического синдрома.
Идиопатический постпрандиальный гипогликемический синдром (то есть возникающий без видимых причин) приобретает клиническое значение, если он развивается при приёме обычного рациона. Диагноз может быть установлен при обнаружении у пациента триады Уиппла после приёма привычной для него пищи (тест со смешанной пищей). Феномен, при котором тест со смешанной пищей не выявляет гипогликемии, называют идиопатическим постпрандиальным (негипогликемическим) синдромом.
Идиопатическая семейная гипогликемия[править | править код]
Идиопати́ческая семе́йная гипогликеми́я (идиопатическая спонтанная гипогликемия, синдром Мак-Куарри) — встречается чрезвычайно редко, носит семейный характер и выявляется в первые 2 года жизни. Патогенетическая основа — повышенная чувствительность к аминокислоте L-лейцину, которая вызывает повышенную секрецию инсулина β-клетками островков поджелудочной железы и снижает скорость глюконеогенеза в печени. Клиническая картина характеризуется частыми гипогликемическими состояниями и вторичными изменениями нервной системы. Тяжесть и частота гипогликемических приступов различны. В межприступный период уровень гликемии колеблется от 2,2 до 6,6 ммоль/л. Проба с лейцином является ценным, но не строго специфическим диагностическим критерием[2].
Гипогликемия новорожденных[править | править код]
Это понятие объединяет гипогликемии, развившиеся у детей в течение первых суток жизни. Гипогликемическое состояние чаще наблюдается у недоношенных новорожденных, родившихся в асфиксии, с наличием признаков дыхательных расстройств, гипотермией. В течение первых 6-ти часов жизни гипогликемия часто развивается у детей, матери которых страдают сахарным диабетом или принимали препараты, снижающие уровень глюкозы в крови. Гипогликемия новорожденных — состояние требующее проведение неотложных лечебных мероприятий независимо от степени выраженности клинических проявлений. Если ликвидировать гипогликемию введением глюкозы (в том числе и внутривенно) не удаётся — применяют дробное введение гидрокортизона или внутримышечное введение глюкагона.[2]
Лечение[править | править код]
Направлено на терапию основного заболевания.
При идиопатическом постпрандиальном синдроме, как правило, эффективно назначение дробного питания с ограничением лекгоусваиваемых углеводов и крепких алкогольных напитков с введением в рацион большого количества клетчатки[1]. Из рациона следует исключить продукты, содержащие лейцин — лабораторный критерий благоприятного течения заболевания уровень гликемии 2,2 и выше[2].
Прогноз[править | править код]
При своевременной диагностике и раннем начале лечения благоприятный.
См. также[править | править код]
- Гипогликемия
- Инсулин
- Инсулинома
- Гипогликемическая кома
- Сахарный диабет
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 Эндокринология (краткий справочник) / Под ред. И. И. Дедова. — 1-е изд. — М.: Рус. врач, 1998. — С. 27. — 95 с. — ISBN 5-7724-0014-2.
- ↑ 1 2 3 Справочник педиатра-эндокринолога / Под ред. М. А. Жуковского. — 1-е изд. — М.: Медицина, 1992. — С. 46. — 304 с. — 20 000 экз. — ISBN 5-225-02616-8.
Ссылки[править | править код]
Источник
Следует также остановиться на аутоиммунном инсулиновом синдроме (АИС) — довольно редкой патологии (в мировой литературе описано несколько сотен наблюдений), которая характеризуется сочетанием рецидивирующих гипогликемических состояний различной степени тяжести с выраженной гиперинсулинемией и высоким титром аутоантител к инсулину при отсутствии в анамнезе экзогенного введения инсулина. Патогенез гипогликемии при АИС определяется обратимым связыванием антителами циркулирующего в плазме инсулина с потерей его биологической активности, вследствие чего, несмотря на постоянно повышенный уровень инсулина в плазме (часто в десятки раз по сравнению с нормой), лабораторные и клинические проявления гипогликемии появляются лишь периодически. Г. А. Мельниченко и соавт. сообщают о случае сочетания АИС с инсулиномой.
Развитие гипогликемических состояний возможно при почечной глюкозурии, диарее, повышении потребности в углеводах во время лактации и беременности (Service F.J.).
Спонтанные гипогликемические состояния — нередкое явление в дебюте развития СД-2, обусловлены функциональным гиперинсулинизмом. Причиной их развития становится снижение чувствительности периферических инсулинзависимых тканей к эндогенному инсулину. Накопление в плазме крови невостребованной тканями глюкозы приводит к гипергликемии (главному стимулу выработки инсулина в ПЖ), которая по механизму обратной связи приводит к выработке b-клетками ПЖ дополнительных порций инсулина и поступлению его в общую систему кровообращения.
В подобной ситуации в плазме крови больного обнаруживаются одновременно избыток и углеводов и С-пептида.
У больных сахарным диабетом необходимо помнить о возможности развития ятрогенных гипогликемии при передозировке инсулина и нероральных сахароснижающих средств, особенно — сульфанилмочевины. Для дифференциации ятрогенной и эндогенной гиперинсулинемии используют исследование в плазме крови уровня С-пептида, который отсутствует в препаратах экзогенного инсулина и является естественной активной формой эндогенного инсулина. Избыток С-пептида определяется при инсулиноме, диффузной гиперплазии островковой ткани, низидиобластозе (перерождение протокового эпителия в инсулинпродуцирующие клетки с явлениями гиперплазии). Избыток сульфанилмочевины определяется но ее концентрации в моче.
Развитие гипогликемических состояний возможно при длительном дефиците питания и кахексии.
Поражения печени различного генеза могут сопровождаться снижением активности процесса гликогенолиза и дефицитом поступления углеводов в плазму крови из печеночных депо с развитием гипогликемических состояний в условиях повышенной потребности в углеводах, например во время нагрузки.

Гипогликемические состояния могут входить в клиническую картину заболеваний и состояний, проявляющихся снижением секреции контринсулярных гормонов — АКТГ и кортизола (надпочечниковая недостаточность различного генеза, болезнь Аддисопа, гипопитуитаризм, гипотиреоз, дефицит соматотропина) (Service F.J.).
Одной из частых причин развития внепанкреатической гипогликемии служит избыточное употребление алкоголя, особенно в сочетании с дефицитом питания. Основные причины гипогликемических состояний представлены ниже.
Причины гипогликемии (Кузин Н.М., Егоров А.В.):
1. Гиперинсулинемия в сочетании с высоким уровнем С-пептида:
— инсулинома;
— островково-клеточная гиперплазия;
— низидиобластоз.
2. Гииеринсулинемия в сочетании с низким уровнем С-пептида:
— эндогенный инсулин;
— ипсулиновый аутоиммунный синдром.
3. Лекарственная сульфанилурия.
4. Лекарственная гиперинсулинемия:
— салицилаты;
— b-блокаторы;
— кинины.
5. Алкоголь (с предшествующим голоданием).
6. Антитела к инсулиновым рецепторам.
7. Опухоли (инсулиноиодобная активность в плазме):
— мезенхимальные опухоли (ретроперитонеальные саркомы);
— гепатомы.
8. Метаболические причины:
— болезни печени;
— болезнь Аддисона;
— болезнь накопления гликогена;
— галактоземия;
— гипопитуитаризм;
— голодание;
— недостаточность СТГ;
— непереносимость фруктозы;
— почечная недостаточность.
Автор — Татьяна Петрова.
— Рекомендуем ознакомиться со статьей «Гипогликемии детского возраста. Синдромы Видемана-Беквита и Кохрейна»
Оглавление темы «Инсулинома и ее проявления»:
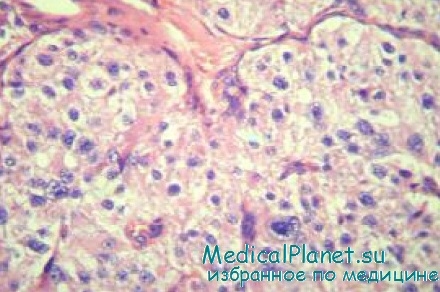
- Инсулинома. Причины и морфология
- Патофизиология инсулиномы. Гипогликемия при инсулиноме
- Неврологические нарушения при инсулиноме. Дифференциация
- Аутоиммунный инсулиновый синдром (АИС). Причины гипогликемии
- Гипогликемии детского возраста. Синдромы Видемана-Беквита и Кохрейна
- Гликогеновые болезни у детей. Гликогенозы
- Нервная система при инсулиноме. Поражение
- Гипогликемическая энцефалопатия (ГЭП). Очаговые нарушения
- Когнитивные расстройства, внимание при инсулиноме
- Электрофизиологические нарушения головного мозга при инсулиноме
Источник
