Болезнь гоше код мкб
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 9 декабря 2014;
проверки требуют 27 правок.
Болезнь Гоше́ (Сфинголипидоз) — наследственное заболевание, является самой распространённой из лизосомных болезней накопления. Развивается в результате недостаточности фермента глюкоцереброзидазы, которая приводит к накоплению глюкоцереброзида во многих тканях, включая селезёнку, печень, почки, лёгкие, мозг и костный мозг. Заболевание связано с рецессивной мутацией в гене GBA, расположенном в 1-ой хромосоме, и поражает как мужчин, так и женщин. Заболевание названо в честь французского врача Филиппа Гоше, который первым описал его в 1882.
Типы болезни Гоше[править | править код]
Болезнь Гоше подразделяется на три основных типа.
Тип I[править | править код]
Болезнь Гоше I (ненейронопатического) типа встречается с частотой 1/50000. Наиболее часто встречается среди ашкеназских евреев. Проявление симптомов начинается в детстве или во взрослом возрасте и включают увеличенную печень и сильно увеличенную селезёнку (что может приводить к её разрыву и дополнительным повреждениям). Возможны слабость костей и выраженные костные заболевания. Изменённые селезёнка и костный мозг вызывают анемию, тромбоцитопению и лейкопению. Хотя мозг при этом типе не повреждается, могут быть нарушения в лёгких и почках. Больные страдают от частых гематом, вызванных тромбоцитопенией, и от постоянной усталости (из-за пониженного числа эритроцитов). Больные могут доживать до взрослого возраста и при умеренной форме симптомы могут отсутствовать.
Тип II[править | править код]
Тип II представляет собой нейронопатическую инфантильную форму. Средний возраст заболевания 3—5 мес. Неврологические осложнения (тяжелые судорожные приступы, гипертонус, апноэ, выраженная задержка умственного развития) проявляются к 6 мес. Симптомы включают гепатоспленомегалию, широкое прогрессирующее повреждение мозга, нарушенную моторику глаз, спастичность, судороги, ригидность конечностей. Больные дети плохо сосут и глотают; обычно умирают в возрасте от одного до двух лет. Частота встречаемости 1/100000, этнической предрасположенности не имеет.
Тип III (подострая нейронопатическая (ювенильная) форма)[править | править код]
Тип 3 может начинаться как в детстве, так и у взрослых с частотой встречаемости 1/100000. У большинства характеризуется медленным прогрессированием и умеренностью неврологических симптомов. Первым неврологическим признаком является, как правило, окуломоторная апраксия, расстройство глазодвигательных функций. По мере прогрессирования заболевания присоединяются атаксия, мышечная спастичность и слабоумие. Наряду с гепатоспленомегалией в патологический процесс вовлекаются и другие органы и системы. Спленомегалия безболезненная и обычно выявляется случайно. Больные доживают до подросткового и взрослого возраста.
Одна из главных причин инвалидизации при 1 и 3 типе болезни Гоше —- поражение костной ткани. Нарушение нормальных физиологических процессов происходит из-за накопления липидов в остеокластах и замещении инфильтратами клеток Гоше нормальных элементов костного мозга. Несмотря на увеличение печени и её дисфункцию, случаи тяжёлой печёночной недостаточности встречаются редко. Чаще встречается относительная портальная гипертензия как следствие фиброза.
Диагностика болезни Гоше[править | править код]
Диагностика болезни Гоше включает комплексную оценку клинической картины, лабораторные тесты и другие исследования (например, УЗИ печени и селезёнки).
Для диагностики болезни Гоше применяются следующие лабораторные исследования:
Определение активности бета-глюкоцереброзидазы (ферментная диагностика)[править | править код]
При болезни Гоше — снижена.
Определение активности хитотриозидаза[править | править код]
При болезни Гоше — повышена.
Секвенирование экзонов и приэкзонных участков интронов гена GBA (ДНК-диагностика)[править | править код]
Идентифицировано значительное количество мутаций гена GBA, приводящих к развитию болезни Гоше[1].
Диагностика болезни Гоше в России[править | править код]
В России ферментную и генетическую диагностику болезни Гоше выполняют в Лаборатории Наследственных болезней обмена веществ МГНЦ РАМН и в Лаборатории молекулярной генетики и медицинской геномики Научного Медицинского Исследовательского Центра здоровья детей Минздрава России.
Дифференциальная диагностика[править | править код]
- с другими лизосомными болезнями накопления: болезнь Ниманна-Пика, болезнь Вольмана, GM1-ганглиозидоз, галатосиалидоз;
- с другими наследственными болезнями обмена: гликогеноз, талассемия, гемофилия, хроническая гранулематозная болезнь;
- c другими заболеваниями: остеомиелит, костный туберкулёз, вирусный гепатит, онкологические заболевания крови.
Лечение[править | править код]
Используемые препараты:
- имиглуцераза (с 1995)[2],
- velaglucerase alfa (с 2010)[3],
- taliglucerase alfa (с 2012)[4],
- элиглустат (с 2014)[5],
- miglustat (с 2003 года)[6]
См. также[править | править код]
- Лизосомные болезни накопления
Примечания[править | править код]
Ссылки[править | править код]
- Лизосомные болезни накопления
- Содействие инвалидам с детства,страдающим болезнью ГОШЕ, и их семьям( межрегиональная общественная организация по России)
Источник
В последние годы особое внимание в нашей стране уделяется проблеме ранней диагностики и лечения орфанных заболеваний.
Редкие (орфанные) заболевания — это встречающиеся с определенной частотой жизнеугрожающие или хронические прогрессирующие заболевания, приводящие без лечения к смерти или пожизненной инвалидизации пациентов. На сегодня в мире их насчитывается более 7,5 тысяч. Большинство из них обусловлено генетическими отклонениями, симптомы многих из них могут быть очевидны уже с рождения или же проявляться в детском, реже в более старшем возрасте. В 2012 г. принят Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», в котором впервые на государственном уровне введено понятие редких (орфанных) заболеваний. В нашей стране к орфанным относятся заболевания, которые имеют распространенность не более 10 случаев заболевания на 100 000 населения (статья 44). Одним из заболеваний, включенных в группу орфанных, является болезнь Гоше (код по МКБ-10 Е75.2 — «Другие сфинголипидозы»).
Болезнь Гоше (БГ) — наиболее частая форма наследственных ферментопатий из группы лизосомных болезней накопления. Тип наследования — аутосомно-рецессивный. Присутствие двух мутантных аллелей гена ассоциируется со значительным снижением (менее 30% от нормального уровня) каталитической активности β-D-глюкозидазы (глюкоцереброзидазы), что приводит к накоплению в лизосомах макрофагов глюкоцереброзида. Ген глюкоцереброзидазы картирован на хромосоме 1q21. Частота БГ в общей популяции составляет 1:40 000–1:60 000; среди евреев-ашкенази (выходцев из Восточной Европы) — 1:450–1:800 [1]. Возраст манифестации заболевания широко варьирует — от рождения до старости.
В зависимости от клинического течения выделяют 3 типа БГ:
- тип 1 — ненейронопатический;
- тип 2 — инфантильный или острый нейронопатический;
- тип 3 — подострый нейронопатический.
Тип 1 является самым частым. В отличие от 2-го и 3-го типов при данном типе нервная система в патологический процесс не вовлекается [1–4].
При БГ 1-го типа основными клиническими проявлениями являются: задержка физического и полового развития, гепатоспленомегалия, геморрагический и астенический синдромы (ассоциированы с тромбоцитопенией, анемией или панцитопенией), нарушение подвижности в суставах, патологические переломы, боли в костях (костные кризы).
Наиболее ранним признаком БГ 1-го типа заболевания является спленомегалия. Селезенка может увеличиваться в размерах в 5–80 раз. По мере прогрессирования заболевания и увеличения размеров органа возможно развитие инфарктов или разрыва селезенки с возникновением фатального кровотечения. Гепатомегалия выражена в меньшей степени и развивается, как правило, в более поздние сроки заболевания, при этом функция печени не страдает. Геморрагический синдром, обусловленный тромбоцитопенией и нарушением функции тромбоцитов, проявляется в виде развития подкожных гематом, повышенной кровоточивости слизистых оболочек, длительных кровотечений после малых оперативных вмешательств, экстракции зубов, меноррагий и пр. Поражение костно-суставной системы может протекать как в виде бессимптомной остеопении и колбообразной деформации дистальных отделов бедренных костей (колбы Эрленмейера), так и в виде тяжелейшего остеопороза, сопровождающегося множественными патологическими переломами и ишемическими некрозами, приводящим к развитию вторичных остеоартрозов и тяжелых необратимых ортопедических дефектов. У трети больных отмечаются хронические боли в костях. Они могут протекать в виде костных кризов — мучительной, интенсивной боли, чаще в области нижних или верхних конечностей, сопровождающейся гиперемией и болезненностью в области суставов, снижением двигательной активности, лихорадкой, ознобом, повышением уровня маркеров воспаления (лейкоцитоз, повышенная скорость оседания эритроцитов).
При БГ 2-го типа клинические симптомы проявляются уже на первом году жизни, часто уже в первое полугодие. Заболевание имеет быстро прогрессирующее течение и характеризуется задержкой психомоторного развития с потерей ранее приобретенных навыков, нарушением глотания, часто осложняющимся аспирационной пневмонией, тризмом, билатеральным фиксированным косоглазием, гиперрефлексией, положительным симптомом Бабинского, прогрессирующей спастичностью с ретракцией шеи, приступами тонико-клонических судорог, резистентных к традиционной противосудорожной терапии, развитием гепатоспленомегалии.
При БГ 3-го типа неврологические проявления сходны с таковыми при БГ 2-го типа, но возникают, как правило, позже (в 5–6 лет и старше) и протекают менее выраженно. Для данного типа характерны окуломоторные расстройства, экстрапирамидная и мозжечковые нарушения, генерализованные тонико-клонические судороги, миоклонии. Снижение интеллекта может проявляться от незначительных изменений вплоть до тяжелой деменции. Течение заболевания медленно прогрессирующее.
Диагностика БГ основывается на выявлении характерных клинических проявлений — задержка физического и полового развития, астенический синдром, повышенная кровоточивость, боли в костях и суставах, гепатоспленомегалия, указание в анамнезе на переломы, реже — неврологическая симптоматика в виде глазодвигательной апраксии или сходящегося косоглазия, атаксии, снижение интеллекта и др., на изменениях в клиническом анализе крови — тромбоцитопения, лейкопения, анемия или панцитопения, наличие признаков гепатоспленомегалии при УЗИ органов брюшной полости, выявление диффузного остеопороза, колбообразной деформации дистальных отделов бедренных и проксимальных отделов большеберцовых костей, очагов остеолизиса, остеосклероза и остеонекроза по данным магнитно-резонансной томографии (МРТ) или рентгенографии костей скелета, патологических переломов. Проведение морфологического исследования костного мозга позволяет выявить клетки Гоше и одновременно исключить диагноз гемобластоза или лимфопролиферативного заболевания как причины цитопении и гепатоспленомегалии.
«Золотым» стандартом диагностики БГ является определение активности β-D-глюкозидазы в лейкоцитах (сухие пятна крови) — при БГ она снижена. Также диагностическим маркером может являться повышение активности хитотриозидазы — гидролитического фермента, синтезируемого активированными макрофагами в сыворотке крови, и ДНК-диагностика.
Основой патогенетического лечения БГ является проведение ферментозаместительной терапии (ФЗТ) (показана при БГ 1-го и 3-го типов). При БГ 2-го типа она не эффективна (препарат не проникает через гематоэнцефалический барьер).
На сегодняшний день на российском фармацевтическом рынке представлены следующие препараты для ФЗТ:
- имиглюцераза — рекомбинантная глюкоцереброзидаза, синтезируемая клеточной линией, полученной из яичников китайских хомячков;
- велаглюцераза альфа — очищенная форма фермента глюкоцереброзидазы, полученная посредством технологии рекомбинантной ДНК линии человеческих клеток.
В связи с гетерогенностью заболевания доза ферментного препарата для каждого больного подбирается индивидуально (от 30–60 ЕД/кг на введение при 1-м типе до 120 ЕД/кг при 3-м типе) и вводится один раз в 2 недели в/в капельно. Доза может повышаться или снижаться в зависимости от степени достижения терапевтического эффекта на основании оценки клинических проявлений.
Важно помнить, что ошибочно и необоснованно при БГ проведение спленэктомии, так как это может привести к развитию тяжелых последствий: цирроза печени, деформаций костей и суставов, костных кризов, фиброза легких, проведению повторных пункций костного мозга и других инвазивных диагностических мероприятий (биопсия печени, селезенки), оперативному лечению костных кризов (часто ошибочно рассматриваются как проявления остеомиелита), назначению кортикостероидов с целью купирования цитопенического синдрома и препаратов железа (анемия при БГ носит характер «анемии воспаления»).
В качестве клинического примера приводится история развития ребенка А., 2004 г. рождения.
Диагноз: болезнь Гоше 3-го типа (E75.2) (гомозиготная мутация L444Р в гене GBA).
Осложнения: смешанный тетрапарез. Симптоматическая фокальная эпилепсия. Косоглазие содружественное сходящееся альтернирующее. Нарушение психоречевого развития. Килевидная деформация грудной клетки. Грудной кифоз III ст. S-образный левосторонний сколиоз II ст. Остеопороз. Гепатоспленомегалия. Вторичная дилатационная кардиомиопатия. НК 0 ст.
Анамнез жизни: мальчик от первой беременности, протекавшей без осложнений, роды срочные, вес при рождении 3330 г, длина 54 см. Раннее развитие без особенностей. В возрасте 2 мес выявлено снижение уровня гемоглобина до 98 г/л, по данным УЗИ — спленомегалия. Ребенок получил два курса терапии препаратами железа, однако значимого эффекта получено не было. С одного года на фоне гипертермии и фебрильных судорог стало отмечаться сходящееся косоглазие.
В возрасте 1 г 3 мес мальчик госпитализирован в гематологическое отделение, где проведена стернальная пункция. В пунктате выявлены клетки Гоше. По данным УЗИ: гепатоспленомегалия (печень +4,5 см, селезенка до +20 см из-под края реберной дуги), в анализе крови снижение уровня гемоглобина до 90 г/л; тромбоцитов — до 114 тыс. Ед/мкл. Образцы крови направлены на генетическое исследование, в результате которого установлено снижение активности фермента β-D-глюкозидазы до 1,8 нМ/мг/час и повышение уровня хитотриозидазы до 951,6 нM/мл/час. Проведена ДНК-диагностика — обнаружена гомозиготная мутация L444Р в гене GBA. Подтвержден диагноз: болезнь Гоше.
В возрасте 1 г 6 мес (04.2006 г.) ребенок начал получать ФЗТ препаратом имиглюцеразы в дозе 40 ед/кг в/в 1 раз в 14 дней. При контрольном обследовании через 6 мес от начала терапии отмечается сокращение размеров печени (до +2,5 см) и селезенки (до +12 см из-под края реберной дуги); нормализация показателей крови (гемоглобин — 121 г/л, тромбоциты — 214 тыс. Ед/мкл). Однако с 5 лет у ребенка стали отмечаться приступы повышенной сонливости с нарушением дыхания, цианозом носогубного треугольника, судорожными движениями рук, гиперсаливацией, повторяющиеся до 5–7 раз в сутки; периодичность приступов составляла 1 раз в 7–10 дней. При обследовании по данным электроэнцефалографии патологии не выявлено, на МРТ головного мозга установлена умеренно выраженная вторичная вентрикуломегалия боковых желудочков. Ребенок консультирован психоневрологом, в терапию добавлены препараты вальпроевой кислоты пролонгированного действия, леветирацетама дигидрохлорида и топирамата. Доза препарата ФЗТ повышена до 120 ед/кг.
За 2 года комплексной терапии, включающей высокие дозы имиглюцеразы, у ребенка улучшились показатели физического развития (рис.), уменьшились размеры печени и селезенки, улучшилась структура их паренхимы, снизился уровень хитотриозидазы (до 527,5 нM/мл/час). Отмечается положительная динамика и со стороны неврологического статуса: исчезновение симптома Грефе, нарастание мышечного тонуса, улучшение координаторных и двигательных навыков, активная наработка словарного запаса (более 20 слов). Однако сохраняется сходящееся косоглазие.
.jpg)
Литература
- Stirnemann J., Belmatoug N., Camou F., Serratrice C. A Review of Gaucher Disease Pathophysiology, Clinical Presentation and Treatments // Int J Mol Sci. 2017, Feb. 17; 18 (2), pii: E441. DOI: 10.3390/ijms18020441.
- Grabowski G. A., Andria G., Baldellou A. et al. Pediatric nonneuronopathic Gaucher disease: presentation, diagnosis and assessment. Consensus statements // Eur J Pediatr. 2004, v. 163, p. 58–66.
- Vellodi A., Bembi B., de Villemeur T. B. et al. Management of neuronopathic Gaucher disease: a European consensus // J Inherit Metab Dis. 2001, v. 24, p. 319–327.
- Болезнь Гоше у детей. Клинические рекомендации. 2016. 28 с.
Т. А. Бокова, доктор медицинских наук, профессор
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
Контактная информация: bta2304@mail.ru
DOI: 10.26295/OS.2019.69.16.003
Болезнь Гоше: орфанное заболевание в практике педиатра/ Т. А. Бокова
Для цитирования: Лечащий врач № 9/2019; Номера страниц в выпуске: 21-23
Теги: ранняя диагностика, ферментопатия, глюкоцереброзидаза
Купить номер с этой статьей в pdf
Источник
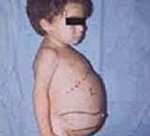
Болезнь Гоше – это генетическое заболевание, характеризующееся нарушением липидного обмена, недостаточностью лизосомальных ферментов, накоплением гликолипидов в клеточных структурах. Симптомы определяются типом патологии. Общими признаками являются увеличение печени, селезенки, снижение свертываемости крови. При I типе выявляются нарушения со стороны костной системы: остеопороз, частые переломы, инфекции костей. При II и III типе доминирует неврологическая симптоматика: судороги, паралич, косоглазие, задержка умственного развития. Диагностика основана на биохимическом анализе дефицитарного фермента. Лечение включает ферментозаместительную, субстратредуцирующую и симптоматическую терапию.
Общие сведения
Заболевание получило свое название по фамилии французского врача Филиппа Гоше. В 1882 году он описал симптомы и патанатомические особенности строения селезенки пациентки, которая умерла от сепсиса. Спустя несколько десятилетий при аналогичном клиническом случае Гоше определил накопление в селезенке глюкоцереброзида и недостаточность фермента глюкоцереброзидазы. Болезнь Гоше (сфинголипидоз, глюкозилцерамидный липидоз) относится к группе лизосомальных болезней накопления – наследственных патологий, при которых изменены функции клеточных органелл лизосом. Частота заболевания составляет от 1:40 тыс. до 1:70 тыс. Распространенность наиболее велика в сообществах, где допустимы браки между близкими родственниками, например, у евреев ашкенази. Носительство мутационного гена определяется примерно у 1 человека из 400.

Болезнь Гоше
Причины
Глюкозилцерамидный сфинголипидоз является наиболее частой формой наследственных ферментопатий. Причиной его развития считается дефект гена GBA, который кодирует фермент лизосом бета-глюкозидазу (глюкоцереброзидазу), ответственную за расщепление липидов. Наследование болезни происходит аутосомно-рецессивным способом, для формирования ферментопатии необходимо присутствие пары измененных генов: один – от матери, другой – от отца. В супружеской паре, где оба родителя – носители мутации, вероятность рождения больного ребенка составляет 25%. Риск передачи одного дефектного гена, то есть риск носительства без развития болезни в таких семьях равен 50%. При наличии в генотипе двух мутантных аллелей функция глюкоцереброзидазы снижается на 15-30% от нормального уровня.
Патогенез
Патогенетической основой болезни является снижение каталитической активности бета-глюкозидазы. В результате нарушается процесс расщепления гликосфинголипидов (сложных соединений липидов и углеводов) до глюкозы и церамида. Аномально прогрессивное накопление макромолекул происходит в клетках, которые характеризуются повышенной скоростью их обновления – в макрофагах. Негидролизованные липиды концентрируются в лизосомах, образуются особые клетки накопления – клетки Гоше. Первичный метаболический сбой провоцирует вторичные расстройства биохимических процессов и клеточных функций. Из-за патологии жирового обмена развивается синдром активации макрофагов. Стимулируется моноцитопоэз, увеличивается содержание макрофагов в печени, селезенке, костном мозге. Это становится причиной спленомегалии, гепатомегалии, инфильтрации костного мозга. Расстройство регуляторной функции макрофагов является провоцирующим фактором цитопении, поражения костей и суставов.
Симптомы болезни Гоше
По возрасту дебюта и особенностям клинической картины выделяют три типа болезни. Первый тип наиболее распространен, имеет хронический характер течения. Симптомы чаще проявляются к 30-40 годам, реже болезнь манифестирует в детском возрасте. Увеличение размеров печени и селезенки начинается сразу после рождения, но клинически проявляется позже. Первыми признаками патологии становятся анемия, повышенная кровоточивость. Угнетение системы кроветворения сопровождается снижением уровня гемоглобина и тромбоцитов. Изменения со стороны опорно-двигательного аппарата представлены болями в костях и суставах, частыми переломами, деформациями (как правило, изменяется бедренная кость). У взрослых заметна гиперпигментация на лице и ногах: кожа темнеет, приобретает оттенок от желтоватого до желто-коричневого. Возможно появление плоских красных пятен с типичной локализацией в области вокруг глаз. Рост пациентов ниже среднего.
Второй тип болезни (острый инфантильный или острый нейропатический) встречается очень редко, развивается в промежутке от рождения до полутора лет, чаще всего симптомы дебютируют в первые три месяца жизни. Характеризуется стремительным течением, плохим откликом на лечение. На первый план выходят неврологические расстройства, спровоцированные скоплением клеток Гоше в центральной нервной системе. Дети слабо кричат, вяло сосут. Нарушен глотательный рефлекс, нередко отмечаются сбои цикла дыхания. Наблюдается заметная задержка психического и физического развития. На начальной стадии заболевания мышечный тонус снижен, через 9-12 месяцев после дебюта возникает гипертонус, особенно в мышцах шеи и конечностях. Развиваются судороги, косоглазие, спастический паралич. Печень и селезенка увеличены. Дети часто болеют тяжелой пневмонией.
Третий тип – ювенильный или подострый нейропатический. Первые признаки – увеличение селезенки и печени – возникают в 2-3 года. Полная симптоматика разворачивается в период с 6 до 15 лет. Клинические проявления поражения ЦНС включают гипертонус мышц, паралич спастического типа, косоглазие, непроизвольные спазмы, судороги, затрудненный цикл дыхания с трудностью вдоха, проблемы при глотании. Имеются расстройства психического развития: снижение интеллектуальных функций, несформированность речи и письма, эмоциональная неустойчивость, психозы. Дети отстают в половом развитии. Течение болезни неуклонно прогрессирующее.
Осложнения
Наиболее тяжелые осложнения выявляются при втором и третьем типе болезни. Поражение спинного и головного мозга приводит к нарушению дыхательного цикла, развиваются внезапные остановки дыхания, возрастает риск спазма гортани и смерти от удушья. Сниженный уровень тромбоцитов способен стать причиной обширных внутренних кровотечений. У больных с патологией первого типа распространенным осложнением является разрушение костей, их повышенная ломкость и инфекционные поражения. Ограничивается подвижность, пациенты не могут передвигаться самостоятельно, нуждаются в постороннем уходе.
Диагностика
Сбор анамнеза и физикальное обследование выполняется врачом-эндокринологом и неврологом, дополнительно назначаются консультации генетика, гематолога, офтальмолога, педиатра, психиатра. Анамнестические данные включают наличие болезни Гоше у родственников. При осмотре выявляются типичные признаки: низкий рост, патологии костей, неврологические симптомы (косоглазие, атаксия, паралич), геморрагический синдром, гиперпигментация кожи. Иногда подозрение на заболевание возникает после случайного выявления увеличенной селезенки на снимках УЗИ, угнетении кроветворной системы по данным общего анализа крови. Для подтверждения диагноза, исключения других метаболических наследственных патологий, остеомиелита, костного туберкулеза, вирусного гепатита и онкологических поражений крови проводится специфическая диагностика:
- Клиническое, биохимическое исследование крови. У большинства больных определяется тромбоцитопения, лейкопения, анемия, которая у детей обычно имеет железодефицитное происхождение. В результатах биохимического анализа обнаруживается сниженная активность глюкоцереброзидазы.
- Ферментный анализ клеток. При болезни Гоше в образцах сухой крови и в фибробластах кожи выявляется недостаточная активность глюкозидазы. Степень дефицитарности фермента не имеет прямой корреляции с выраженностью симптомов. Дополнительный биохимический маркер – хитотриозидаза. Этот фермент синтезируется активированными макрофагами, характерно повышение его активности в 6-10 раз.
- Морфологическое изучение костного мозга. Подтверждается наличие специфических для данного заболевания структур – клеток Гоше. Результат позволяет исключить гемобластоз и лимфопролиферативное заболевание.
- Исследование структуры костной ткани. С целью оценки тяжести поражения костно-суставной системы выполняется денситометрия, рентгенография и/или МРТ костей скелета. Возможен диффузный остеопороз, могут визуализироваться колбы Эрленмейера, очаги остеолизиса, остеосклероза и остеонекроза. На ранних стадиях болезни отмечается остеопения, инфильтрация костного мозга.
- Визуализирующее исследование селезенки, печени. Проводится УЗИ и МРТ внутренних органов. По результатам устанавливается наличие или отсутствие очаговых поражений, измеряется объем увеличенного органа. Исходные показатели в последующем позволяют контролировать эффективность терапии.
- Молекулярно-генетические исследования. ДНК-диагностика является необязательной процедурой. Подтверждение мутации в гене GBA бывает необходимо при неоднозначности биохимических исследований, а также в рамках пренатальных и преимплантационных обследований.
Лечение болезни Гоше
Специализированная помощь больным с первым и третьим типом болезни направлена на устранение симптомов и компенсацию первичного генетического дефекта – увеличение количества недостающего фермента, усиление катаболизма гликосфинголипидов. При 2 типе патологии терапевтические мероприятия оказываются недостаточно эффективными, усилия врачей сводятся к облегчению клинических проявлений – болей, судорог, дыхательных расстройств. Общая схема включает следующие направления:
- Ферментозаместительная терапия. Основным методом лечения является пожизненная ферментная заместительная терапия (ФЗТ) с применением рекомбинантной глюкоцереброзидазы. Эффективность достаточно высока – симптомы полностью купируются, качество жизни больных повышается. ФЗТ целесообразна при третьем и первом типе заболевания. Препараты вводятся внутривенно. Частые инфузии иногда становятся причиной воспалительных заболеваний вен (флебитов).
- Субстрат-редуцирующая терапия. Данное направление является новым в лечении болезни Гоше, относительно широко распространено в США и странах Европы. Нацелено на снижение скорости производства субстрата гликосфинголипидов и ускорение катаболизма накапливающихся макромолекул. В качестве препаратов выступают специфические ингибиторы глюкозилцерамидсинтазы. Метод показан при заболевании 1 типа с легкими и умеренными симптомами.
- Симптоматическая терапия. При явлениях остеопороза назначается комплексная терапия, включающая прием кальцийсодержащих препаратов, витамина D и соблюдение диеты, обогащенной кальцием. Эти меры позволяют замедлить потерю костной массы, повысить прочность костей, предотвратить переломы. При скелетных осложнениях применяются анальгезирующие средства (НПВС), антибактериальная терапия. Симптомы неврологических нарушений купируются противоэпилептическими препаратами, ноотропами, миорелаксантами.
Прогноз и профилактика
Благоприятный исход наиболее вероятен у пациентов с 1 типом заболевания – комплексный терапевтический подход позволяет нормализовать функциональность глюкоцереброзидазы, предупредить развитие осложнений, избежать инвалидизации. При 3 типе прогноз зависит от характера течения болезни, индивидуальной реакции организма на лечебные мероприятия. 2 тип имеет крайне тяжелые проявления и завершается гибелью больного. Профилактика проводится во время планирования беременности и на ее начальных сроках. Медико-генетическое консультирование рекомендуется семьям, имеющим близких родственников с данной патологией. При высоком риске передачи мутации будущему ребенку в первом триместре выполняется исследование уровня фермента в амниотической жидкости, решается вопрос о прерывании беременности.
Источник
