Аспирационный синдром у новорожденных клинические рекомендации
Год утверждения 2016
Профессиональные ассоциации:
- Российская ассоциация специалистов перинатальной медицины
- Российское общество неонатологов
Оглавление
1. Краткая информация
2. Диагностика
3. Лечение
4. Реабилитация
5. Профилактика
1. Краткая информация
1.1 Определение
Синдром дыхательных расстройств новорожденного или «респираторный дистресс-синдром» (РДС) — обусловленное первичным дефицитом сурфактанта и незрелостью лёгких расстройство дыхания у детей в первых дней жизни.
Частота РДС выше при меньшем гестационном возрасте и массе тела.
1.2 Этиология и патогенез
Основные причины РДС:
- нарушение синтеза и экскреции сурфактанта, обусловленное функциональной и структурной незрелостью лёгочной ткани;
- дефект структуры сурфактанта (крайне редко).
1.3 Эпидемиология
1.4 Код по МКБ — 10
Р22.0 — Синдром дыхательного расстройства у новорожденного.
1.5 Классификация
Нет.
1.6 Клиническая картина
- Одышка в первые минуты/часы жизни;
- Экспираторные шумы («стонущее дыхание»);
- Западение грудной клетки на вдохе с напряжением крыльев носа, раздуванием щек (дыхание «трубача»);
- Цианоз;
- Ослабление дыхания, крепитирующие хрипы.
- Нарастающая потребность в дополнительной оксигенации.
2. Диагностика
2.1 Жалобы и анамнез
Факторы риска
Предрасполагающие факторы:
- РДС у сибсов;
- Гестационный диабет и СД 1 типа матери;
- Гемолитическая болезнь плода;
- Преждевременная отслойка плаценты;
- Преждевременные роды;
- Мужской плод и преждевременные роды;
- Кесарево сечение до начала родовой деятельности;
- Асфиксия новорожденного.
2.2 Физикальное обследование
Оценка дыхательной недостаточности по шкале Сильверман (Silverman) для определения эффективности проводимой респираторной терапии или показания для ее начала.
2.3 Лабораторная диагностика
Всем новорожденным с дыхательными нарушениями в первые часы жизни:
- анализы крови на кислотно-основное состояние, газовый состав;
- уровень глюкозы;
- маркеры инфекционного процесса (прокальцитонин);
- клинический анализ крови с нейтрофильным индексом дважды с интервалом 48 часов;
- СРБ дважды с интервалом 48 часов;
- микробиологический посев крови.
При РДС отрицательные маркеры воспаления и микробиологическое исследование.
2.4 Инструментальная диагностика
Рентгенологическое исследование всем новорожденным с дыхательными нарушениями в первые сутки жизни.
Рентгенологическая картина при РДС от уменьшения пневматизации до «белых лёгких».
Характерные признаки РДС:
- диффузное снижение прозрачности лёгочных полей,
- ретикулогранулярный рисунок,
- полоски просветлений в корнях легкого (воздушная бронхограмма).
Изменения неспецифичны и возможны при раннем неонатальном сепсисе и врожденной пневмонии.
2.5 Иная диагностика
Дифференциальная диагностика
- Транзиторное тахипноэ;
- Ранний неонатальный сепсис, врожденная пневмония;
- Синдром мекониальной аспирации;
- Синдром утечки воздуха, пневмоторакс;
- Персистирующая легочная гипертензия;
- Аплазия/гипоплазия легких;
- Врождённая диафрагмальная грыжа.
3. Лечение
3.1 Консервативное лечение
3.1.1 Профилактика гипотермии в родильном зале у недоношенных новорожденных
Основные мероприятия по тепловой защите проводятся в первые 30 секунд жизни.
Объём мероприятий различается у недоношенных более 28 недель более 1000 г массы и у детей с массой тела менее 1000 г. до 28 недель.
3.1.2 Отсроченное пережатие и пересечение пуповины и сцеживание пуповины
У недоношенных новорожденных с ОНМТ и ЭНМТ пережатие и пересечение пуповины через 60 секунд после рождения значительно снижает частоту:
- некротического энтероколита;
- ВЖК;
- сепсиса;
- потребность в гемотрансфузиях.
Решение о пересечении принимается коллегиально акушерами-гинекологами и неонатологами.
Альтернатива при невозможности отсроченного пережатия и пересечения пуповины — сцеживание пуповины.
3.1.3 Неинвазивная респираторная терапия в родильном зале
Недоношенным до 32 недель со спонтанным дыханием предпочтительна стартовая СРАР терапия с давлением 6-8 см Н2О.
Недоношенным более 32 недель СРАР проводят при дыхательных нарушениях.
Продленный вдох:
- при отсутствии дыхания;
- дыхании типа «гаспинг»;
- нерегулярном дыхании.
Обязательное условие «продленного вдоха» лёгких — регистрация показателей ЧСС и пульсоксиметрия SрО2.
При отсутствии самостоятельного дыхания и/или при сохраняющейся брадикардии — начало ИВЛ маской с последующим:
- переходом на СРАР при восстановлении дыхания/ЧСС;
- интубацией при отсутствии дыхания и/или сохраняющейся брадикардии;
- другой алгоритм.
СРАР в родзале осуществляется:
- аппаратом ИВЛ с функцией СРАР;
- ручным аппаратом ИВЛ с Т-коннектором;
- различными системами СРАР.
СРАР проводиться при помощи:
- лицевой маски;
- назофарингеальной трубки;
- интубационной трубки;
- биназальных канюль.
Противопоказания к СРАР в родильном зале:
- атрезия хоан или другие пороки развития ЧЛО;
- пневмоторакс;
- врожденная диафрагмальная грыжа;
- несовместимые с жизнью врожденные пороки;
- кровотечение.
3.1.4 Инвазивная респираторная терапия в родильном зале
Интубация трахеи и ИВЛ при неэффективности СРАР и ИВЛ маской.
Для эффективной ИВЛ у глубоко недоношенных необходимы:
- контроль давления в дыхательных путях;
- поддержание Реер +5-6 см Н2О;
- возможность плавной регулировки концентрации кислорода от 21 до 100%;
- непрерывный мониторинг ЧСС и SрO2.
Стартовые параметры ИВЛ:
- Pip – 20-22 см Н2О,
- Рeep – 5 см Н2O,
- ЧД 40-60 в минуту.
Основной показатель эффективности ИВЛ — возрастание ЧСС>100 уд/мин.
Устройства для индикации СО2 в выдыхаемом воздухе быстро и надежно подтвердят корректное расположение интубационной трубки.
3.1.5 Оксигенотерапия и пульсоксиметрия
С первой минуты жизни мониторинг ЧСС и SрО2 пульсоксиметрия недоношенных в родильном зале.
Основные точки приложения пульсоксиметрии:
- с первых минут жизни непрерывный мониторинг ЧСС;
- предупреждение гипероксии SрО2 не более 95%;
- предупреждение гипоксии с SрО2 не менее 80% к 5 минуте жизни и не менее 85% к 10 минуте.
Стартовая респираторная терапия у детей до 28 недель гестации и менее с FiО2 = 0,3.
Респираторная терапия у детей большего гестационного возраста осуществляется воздухом.
С конца 1-й минуты жизни ориентироваться на показатели пульсоксиметра.
Концентрацию дополнительного О2 меняют ступенчато на 10-20% каждую последующую минуту до достижения целевых показателей.
Одновременно с началом непрямого массажа сердца концентрацию О2 увеличивают до 100%.
Далее при дополнительной оксигенации недоношенного SpO2 поддерживается на 90-94%.
3.1.6 Сурфактантная терапия
Ведение сурфактанта недоношенным с РДС независимо от массы тела.
Профилактически, в первые 20 минут жизни при сроке гестации 26 недель и менее, если мать не получила полный курс антенатальной профилактики стероидами.
Первые 20 минут жизни при гестационном возрасте >30 недель и потребности в интубации в родильном зале.
Первые 2 часа жизни недоношенного гестации >30 недель, потребности в интубации в родильном зале и зависимости от FiО2 >0,3-04.
Недоношенному на стартовой СРАР в родильном зале при потребности в FiО2 0,5 и более для достижения SpО2 = 85% к 10 минуте жизни и сохранении дыхательных нарушений, а также для улучшения оксигенации в последующие 10-15 минут.
К 20-25 минуте жизни необходимо принять решение о введении сурфактанта или транспортировке в ОРИТН на СРАР.
Метод введения сурфактанта на стартовой терапии СРАР в родильном зале:
- малоинвазивный при сроке гестации ≤ 28 недель;
- традиционный при гестации более 28 недель.
Метод введения сурфактанта малоинвазивный/ INSURE в отделении реанимации родившимся на сроке ≤ 35 недель, на СРАР/неинвазивной ИВЛ при >3 баллах по шкале Сильверман в первые сутки и/или потребности в FiО2 до 0,35 1000 г.
Повторное введение сурфактанта после рентгенографии ОРК при гестации ≤35 недель малоинвазивным /INSURE методом:
- на СРАР при переводе на ИВЛ из-за нарастания дыхательных нарушений (FiO2 до 0,3 у пациентов <1000г и до 0,4 у детей >1000г) в первые сутки жизни;
- на ИВЛ при ужесточении параметров вентиляции: МАР до 7 см Н2О и FiO2 до 0,3 у пациентов 1000г в первые сутки жизни.
Третье введение может быть показано детям на ИВЛ с тяжелым РДС.
Интервалы между введениями 6 часов или меньше при нарастании потребности в FiО2 до 0,4.
Разрешены к применению в РФ:
- Порактант альфа – наиболее эффективный
- Бовактант
- Берактант
- Сурфактант БЛ.
Сурфактант может использоваться при врожденной пневмонии у недоношенных.
3.1.7 Неинвазивная респираторная терапия в ОРИТН
Неинвазивная респираторная терапия в сочетании с сурфактантной по показаниям у недоношенных с дыхательными нарушениями.
Оптимальная стартовая неинвазивная респираторная поддержка — неинвазивная ИВЛ через назальные канюли или маску.
Показания:
- стартовая терапия после профилактического малоинвазивного введения сурфактанта без интубации;
- терапия недоношенных после экстубации;
- резистентные к СРАР и кофеину апноэ;
- у недоношенных на СРАР нарастание дыхательных нарушений до 3 баллов и более выше по шкале Сильвермана и/или увеличение потребности в FiО2 >0,4.
Противопоказания:
- шок;
- судороги;
- легочное кровотечение;
- синдром утечки воздуха,
Стартовые параметр для устройств с открытым контуром (вариабельный поток):
- Pip 8-10см Н2О;
- Peep 5-6 см Н2О;
- ЧД 20-30 в минуту;
- Время вдоха 0,7-1,0 секунда.
Стартовые параметры для устройств с полузакрытым контуром (постоянный поток):
- Pip 12-18 см Н2О;
- Peep 5 см Н2О;
- ЧД 40-60 в минуту;
- Время вдоха 0,3-0,5 секунды.
Снижение параметров при использовании неинвазивной ИВЛ:
- для терапии апноэ – снижение частоты искусственных вдохов;
- для коррекции дыхательных нарушений – снижение Pip.
Дальнейший перевод с неинвазивной ИВЛ на СРАР и на дыхание без респираторной поддержки.
Показания для перевода с неинвазивной ИВЛ на традиционную ИВЛ:
- PaCO2 > 60 мм рт.ст.
- FiО2 ≥ 0,4
- Оценка по шкале Сильверман 3 балла и выше.
- Апноэ, повторяющиеся более 4 раз в течение часа.
- Синдром утечки воздуха, судороги, шок, легочное кровотечение.
При отсутствии аппарата неинвазивной ИВЛ для стартовой неинвазивной респираторной поддержки применяется метод спонтанного дыхания через назальные канюли при постоянном положительном давлении в дыхательных путях.
У глубоко недоношенных новорожденных СРАР с вариабельным потоком имеет некоторое преимущество перед системами с постоянным потоком.
Канюли для СРАР должны быть максимально широкими и короткими.
Показания для поддержки спонтанного дыхания новорожденного с помощью назального CPAP:
- недоношенные с гестационным возрастом 32 недели и меньше профилактически в родзале;
- при гестационном возрасте более 32 недель с самостоятельным дыханием и более 3 баллов по шкале Сильверман.
Противопоказания:
- шок;
- судороги;
- легочное кровотечение;
- синдром утечки воздуха.
Стартовые параметры СРАР:
- 5-6 cm H2O,
- FiO2 0,21-0,3.
Повышение потребности в FiO2 более 0,3 у детей менее 1000г и более 0,35-0,4 у детей более 1000г в первые сутки жизни — показание для малоинвазивного/ INSURE введения сурфактанта.
Отмена СРАР — при снижении давления в дыхательных путях до 2 и менее смН2О и отсутствии потребности в дополнительной оксигенации.
Высокопоточные канюли 4-8 л/мин — альтернатива СРАР у некоторых детей при отлучении от респираторной терапии.
3.1.8 Искусственная вентиляция легких у недоношенных с РДС
Проведение ИВЛ через интубационную трубку при неэффективности респираторной поддержки.
Показания для перевода на ИВЛ:
- неэффективность неинвазивных методов респираторной поддержки;
- тяжелые сопутствующие состояния (шок, судорожный статус, легочное кровотечение).
Продолжительность ИВЛ должна быть минимальной.
ИВЛ проводится с контролем дыхательного объёма, что сокращает её длительность и минимизирует частоту БЛД и ВЖК.
Гипокарбия и тяжелая гиперкарбия способствуют повреждению мозга.
При отучении от респиратора допустима умеренная гиперкарбия при рН артериальной крови выше 7,22.
При отучении от ИВЛ используется кофеин.
Для снижения частоты БЛД кофеин следует назначать с рождения всем детям массой менее 1500г, нуждающимся в респираторной терапии.
Для более быстрого отучения от ИВЛ после 1-2 недель жизни возможен короткий курс малых доз дексаметазона.
Не рекомендуется рутинная седация и аналгезия всем детям на ИВЛ.
Показание для перевода на высокочастотную осцилляторную (ВЧО) ИВЛ:
- потребность в дополнительной оксигенации до 45-50%;
- давление к концу вдоха до 25 см Н2О и выше у недоношенных.
3.1.9 Антибактериальная терапия
Новорожденным при РДС не рекомендуется антибактериальная терапия.
В первые 48-72 часа жизни целесообразна антибактериальная терапия с последующей быстрой отменой при дифференциальной диагностики РДС с врожденной пневмонией или ранним неонатальным сепсисом.
Антибактериальная терапия при дифференциальной диагностике возможна:
- детям с массой менее 1500 г;
- детям на инвазивной ИВЛ;
- при сомнительных маркерах воспаления в первые часы жизни.
Препараты выбора:
- комбинация антибиотиков пенициллинового ряда и аминогликозидов;
- один антибиотик широкого спектра из группы защищенных пенициллинов.
Аамоксициллин+клавулоновая кислота противопоказана из-за неблагоприятного воздействия на кишечную стенку у недоношенных.
3.2 Хирургическое лечение
Хирургическое лечение не существует.
4. Реабилитация
Нет.
5. Профилактика и диспансерное наблюдение
При угрозе преждевременных родов транспортировка в акушерские стационары II – III уровня с отделением реанимации новорожденных.
При угрозе преждевременных родов на 32 неделе и ранее транспортировка в стационар III уровня (перинатальный центр).
При угрозе преждевременных родов на сроке 23-34 недели для профилактики РДС, ВЖК и НЭК показан курс кортикостероидов.
Схемы внутримышечной пренатальной профилактики РДС:
- Бетаметазон 12 мг 2 дозы через 24 часа;
- Дексаметазон 6 мг 4 дозы через 12 часов.
Максимальный эффект достигается через 24 часа и продолжается неделю.
Повторный курс при повторной угрозе преждевременных родов на сроке менее 33 недель проводится через 2-3 недели.
При плановом кесаревом сечении из-за отсутствия родовой деятельности при сроке 35-36 недель рекомендуется кортикостероидная терапия.
При угрозе преждевременных родов на ранних сроках короткий курс токолитиков:
- позволит транспортировку беременной в перинатальный центр,
- даст завершить курс антенатальной профилактики РДС кортикостероидами.
При преждевременном разрыве плодных оболочек показана антибактериальная терапия.
Источник
Синдром аспирации мекония – состояние острой дыхательной недостаточности вследствие внутриутробного попадания в легкие ребенка мекониальных масс с закупоркой просвета бронхов. Характерен синюшный оттенок кожи с рождения, тяжелое шумное дыхание с западением уступчивых мест груди. Состояние расценивается как тяжелое. Синдром аспирации мекония диагностируется на основании внешних признаков дыхательной недостаточности, физикального осмотра и рентгенографической картины. Лечение комплексное, направлено на механическое очищение бронхиального дерева, усиленную оксигенацию и борьбу с инфекционными осложнениями.

Общие сведения
Синдром аспирации мекония – поражение легких новорожденного с высокой вероятностью летального исхода. Смертность достигает 10%, связана с массивной аспирацией мекониальных масс и развитием септического состояния. Частицы первородного кала определяются в амниотической жидкости у 5-20% рожениц, однако заболевание возникает не всегда. Синдром аспирации мекония встречается с частотой около 2-4%. Обычно развивается у доношенных и переношенных детей, у недоношенных встречается реже в связи с особенностями нервной системы, практически исключающими пассаж мекония в околоплодные воды. Является одной из важнейших проблем современной педиатрии в связи с многофакторностью развития и трудностями терапии. В частности, нередко необходимо длительное нахождение ребенка на ИВЛ, что может служить дополнительной причиной развития резистентных к лечению пневмоний.

Синдром аспирации мекония
Причины синдрома аспирации мекония
Хотя этиология состояния продолжает изучаться, большинство исследователей склоняются к гипоксической природе синдрома аспирации мекония. Недостаток кислорода, который возник внутриутробно или в процессе родов, рефлекторно повышает тонус парасимпатической нервной системы. Одновременно происходит централизация кровоснабжения, то есть перераспределение крови с преимущественной циркуляцией в жизненно важных органах (сердце, легкие, мозг) в ущерб всем остальным органам и системам, в том числе кишечнику. Эти два фактора в сумме приводят к гипоксии сосудов брыжейки и рефлекторному расслаблению гладкой мускулатуры кишечника. Как следствие, происходит пассаж первородного кала в околоплодные воды с дальнейшим попаданием в легкие.
Существует большое количество возможных причин гипоксии. Чаще всего дефицит поступления кислорода связан с патологией плаценты, поскольку именно плацентарный кровоток является источником кислорода во внутриутробном периоде развития. Как правило, речь идет о хронической фетоплацентарной недостаточности, обусловленной соматическими заболеваниями матери (в частности, сахарным диабетом и артериальной гипертензией), патологией сосудов плаценты и т. д. Второй вариант – это патологии пуповины или механическое сдавление дыхательных путей (обвитие), что также запускает описанные выше механизмы, приводящие к появлению мекония в околоплодных водах. Определенную роль играет большой вес плода и малое количество амниотической жидкости.
Симптомы и диагностика синдрома аспирации мекония
Синдром аспирации мекония может развиваться с первых минут жизни или спустя несколько часов и даже дней после периода мнимого благополучия. Во многом это зависит от того, как долго малыш испытывал гипоксию, находясь в утробе матери. При раннем появлении симптомов ребенок начинает испытывать трудности с дыханием сразу после рождения. Малыш тяжело и шумно дышит, заметно западение надключичных ямок, межреберных промежутков и других уступчивых мест грудной клетки. Внешне ребенок цианотичный, беспокойный, в тяжелых случаях нервная система, наоборот, угнетена, и пациент выглядит заторможенным. При отсроченном начале синдрома аспирации мекония наблюдаются те же симптомы, но время их возникновения приходится на более поздний период.
Первичная диагностика возможна еще в процессе планового обследования во время беременности. Кардиотокография плода отчетливо показывает затруднение дыхания малыша, в подобных случаях необходимо дальнейшее обследование и поиск причин гипоксии, в частности – анализ амниотической жидкости для выявления в ней частиц мекония. Возможно решение вопроса о досрочном родоразрешении. В процессе интранатальной диагностики синдрома аспирации мекония обращает на себя внимание зеленоватый цвет околоплодных вод, иногда частицы мекония удается визуализировать. Также часто наблюдается зеленоватый цвет ногтей, кожи и пуповины малыша, что, как правило, свидетельствует в пользу длительной внутриутробной гипоксии и тяжелого течения синдрома аспирации мекония.
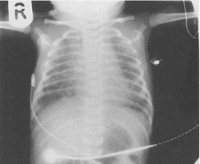
Аускультативно педиатр прослушивает разнокалиберные хрипы, при перкуссии легких участки приглушения чередуются с участками с коробочным звуком. Данные физикального осмотра подтверждаются рентгенографически. На снимке определяются участки ателектаза (спадания альвеол) и эмфиземы (патологического расширения дистальных отделов легких). Такая картина является следствием механической закупорки частицами мекония просвета мелких бронхов, а также вторичного воспалительного процесса, обусловленного токсичностью мекониальных масс. В тяжелых случаях на рентгенограмме обнаруживается так называемая «снежная буря», когда почти вся поверхность альвеол спадается, и остается множество эмфизематозно расширенных участков, неспособных обеспечить циркуляцию воздуха.
Лечение синдрома аспирации мекония
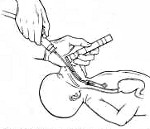
Если синдром аспирации мекония диагностируется еще до родов, то уже в процессе родоразрешения, когда рождается головка, необходимо произвести отсасывание специальным катетером Де Ли. Одна только эта манипуляция, выполненная как можно раньше, позволяет частично освободить верхние дыхательные пути и значительно улучшить оксигенацию. После рождения пациентам с синдромом аспирации мекония проводится лаваж (введение физиологического раствора в трахею с последующим отсасыванием до чистого отделяемого). При наличии выраженной дыхательной недостаточности показано подключение новорожденного к системе ИВЛ.
Важно учитывать, что к моменту подключения ИВЛ легкие должны быть очищены, поскольку в противном случае возможно продвижение оставшихся частиц мекония в дистальные отделы с последующим усугублением дыхательной недостаточности. С целью более быстрого расправления участков ателектаза назначается сурфактант, иногда – оксид азота. Обязательно применение антибиотиков, поскольку частым осложнением синдрома аспирации мекония является аспирационная пневмония. В наиболее тяжелых случаях выполняется экстракорпоральная мембранная оксигенация. Все манипуляции проводятся в отделении реанимации.
Прогноз и профилактика синдрома аспирации мекония
Основным фактором, провоцирующим развитие синдрома аспирации мекония, является внутриутробная гипоксия, поэтому все профилактические мероприятия проводятся в период беременности. Необходима своевременная диагностика и лечение фетоплацентарной недостаточности и соматических заболеваний матери. Стоит избегать перенашивания, которое также повышает риск синдрома аспирации мекония. Прогноз заболевания неблагоприятный. Летальность составляет 10%, выжившие дети в дальнейшем часто имеют хронические легочные патологии. Возможно отставание в развитии вследствие длительной гипоксии.
Синдром аспирации мекония — лечение в Москве
Источник
