Аспирационный синдром у детей описание легких аускультация

 В предлагаемой читателю статье обсуждаются вопросы диагностики и интенсивной терапии аспирационного синдрома. Приводятся как литературные данные, так и собственные наблюдения. Положительные результаты, полученные авторами, позволяют надеяться на внедрение предложенных методик в практику.
В предлагаемой читателю статье обсуждаются вопросы диагностики и интенсивной терапии аспирационного синдрома. Приводятся как литературные данные, так и собственные наблюдения. Положительные результаты, полученные авторами, позволяют надеяться на внедрение предложенных методик в практику.
Аспирационный гиперергический пневмонит был описан американским акушером-гинекологом C. L. Mendelson еще в 1946 году. С тех пор этот синдром получил имя автора. Справедливости ради, следует упомянуть работу группы исследователей из Йельского университета под руководством декана медицинского факультета этого учебного заведения, профессора патанатомии Winternitz M.C., которые еще в 1920 году провели серию экспериментов на себе с эндобронхиальной инсуфляцией серной кислоты. Полученные ими результаты выявили сходство между повреждением легочной ткани при вдыхании боевых отравляющих веществ и развитием аспирационной пневмонии.
Классики на то и классики, чтобы каждое слово их публикаций повторялось, а порой и перевиралось потомками. Итак, напомним еще раз читателю, что аспирационный гиперергический пневмонит (АГП) или синдром Мендельсона развивается при попадании желудочного содержимого с рН ниже 2,5 и объемом более 25 мл в трахею и бронхи. Чем ниже рН и чем больше объем аспирируемой жидкости, тем тяжелее течение аспирационного пневмонита!
Не претерпели значительных метаморфоз и причины аспирационного синдрома:
- Полный желудок (прием пищи в пределах 4-6 часов (при беременности при любом сроке приема пищи), хирургические заболевания органов брюшной полости, ОПН, сахарный диабет, черепно-мозговая травма, коматозное состояние, медикаментозный сон.
- Снижение внутригрудного давления (ИВЛ с отрицательным давлением в конце выдоха, ручная ИВЛ).
- Снижение тонуса кардиального жома (во время беременности, заболевания ЖКТ, медикаментозная депрессия – атропин, миорелаксанты, изжога, пищеводный рефлюкс, запоры).
- Повышение внутрибрюшного давления (беременность, ожирение, заброс воздуха в желудок, фибрилляция мышц, парез кишечника).
Во время анестезиологического пособия мы чаще всего сталкивались с аспирацией в период индукции при многократных попытках интубации трахеи и лишь в небольшом проценте случаев при нарушении герметичности манжеты эндотрахеальной трубки и несоответствии диаметра трахеи размеру интубационной трубки.
Два основных варианта патогенеза синдрома, описанные классиками жанра, позволили потомкам лишь «творчески» дополнить патогенез украшениями типа «каскад эйкозаноидов» и оценкой влияния фактора некроза опухолей.
Как известно, в первом случае в дыхательные пути попадают крупные частицы непереваренной пищи с желудочным соком, как правило, нейтральной или слабокислой реакции. Происходит механическая закупорка дыхательных путей на уровне средних бронхов и возникает клиника острой дыхательной недостаточности (ОДН).
При втором варианте (у беременных встречается гораздо чаще!) в дыхательные пути аспирируется кислый желудочный сок, что вызывает химический ожог слизистой трахеи и бронхов с последующим быстрым развитием отека слизистой, с формированием в конечном итоге бронхиальной обструкции. Приведенная ниже схема позволит читателю наглядно представить некоторые звенья патогенеза.

И вот тут-то наступает момент, когда патогенез превращается в танатогенез.

Клиника аспирационного синдрома
Хорошо, если родителям будущего анестезиолога в первые 7 лет домашнего воспитания удалось привить ребенку честность – одну из наиболее ценных черт характера и добродетелей человека.
Если же на порядочность доктора рассчитывать не приходится, на мысль о развитии авиационного синдрома, должна наводить внезапно pазвившаяся клиника острого астмоподобного приступа с цианозом, одышкой, тахикардией, свистящим дыханием и выслушиваемыми при аускультации многочисленными хрипами в легких с грубыми рентгенологическими признаками субтотальной пневмонии, развившейся в ближайшие часы после операции. Присоединяющиеся инфекционные осложнения, зачастую с анаэробной флорой, являются определяющими факторами в прогнозе.
Диагностические критерии в литературе описаны достаточно чётко:
- Наличие содержимого желудка в трахее.
- Появление дополнительных дыхательных шумов при аускультации легких.
- Повышение сопротивления вдоху (в зависимости от выраженности бронхоспазма до 30-40 см водн. ст. и более).
- Артериальная гипоксемия или увеличение А-аDО2.
- «Снежная буря» при рентгенографии легких.
Обследование должно обязательно включать:
- Экстренную бронхоскопию.
- R-графию легких в динамике.
- ЭКГ.
- ЦВД.
- КЩС и газы крови.
- Лейкоцитарную формулу.
- Биохимию крови.
Разрабатывая лечебную концепцию при данной патологии, мы решили вспомнить о том, что все начинается с химического ожога. Если так, то азбучные истины комбустиологии гласят, что оказание первой помощи при химических ожогах кожи включает:
- Скорейшее удаление химического вещества с пораженной поверхности.
- Снижение концентрации его остатков на коже за счет обильного промывания водой.
- Охлаждение пораженных участков.
Чем раньше и качественнее будет проведена первичная хирургическая обработка, тем лучше результаты!
Именно поэтому блок местного лечения, по нашему мнению, должен выглядеть следующим образом:
- Лаваж легких проводят несколько раз охлажденным (до 10-15° С) физиологическим раствором 10-15 мл через интубационную трубку до полного очищения.
- Экстренная бронхоскопия. Целенаправленное промывание трахеобронхиального дерева охлажденным (до 10-15° С) физиологическим раствором.
- При бронхоскопии метипред вводится локально в зависимости от интенсивности гиперемии 500 – 750 мг.
- Лидокаин 80 мг 1% раствора – местно в зону гиперемии.
Среди вышеперечисленных методов особое значение придаем экстренной бронхоскопии. Если санация начиналась в первые 30 минут после аспирации, то длительность ИВЛ не превышала 4 часов, при выполнении санационной бронхоскопии в течении первых 2 часов длительность ИВЛ возрастает до суток и более.
Если говорить о респираторной поддержке, то мы придерживаемся рутинных, хорошо известных каждому специалисту принципов:
- ИВЛ режим ПДКВ + 9-10 см вод. ст под контролем гемодинамики вначале 100% кислородом с последующим плавным снижением FiO2.
- Максимально допустимое давление вдоха не должно превышать 25 см вод. ст.
- Протективная ИВЛ (5-6 мл/кг массы).
- Перевод на спонтанное дыхание в соответствии с клиникой через режим pressure support.
- Перед экстубацией – проба на адекватность газообмена (самостоятельное дыхание воздухом не менее 30 мин).
Особое значение придаем бронхолитической терапии, которую считаем необходимым проводить следующим образом:
- Алупент (бриканил) капельно 0,5-1,5 мг/сутки перфузором.
- Ингаляция севорана до 1 об%.
- Эуфиллин 240-480 до 960 мг мг/сутки.
- В дальнейшем – перкуссионный массаж, обертывания 15% димексидом, бронхо- и муколитики в терапевтических дозировках.
Кроме того:
- Тиенам 1 г в/в и 1 г в интубационную трубку. Возможно назначение роцефина, меронема.
- Высокие дозы стероидов (метилпреднизолон до 3 г/сутки). О пользе преднизолона, увеличении выживаемости при их раннем назначении свидетельствуют и A.Lee с соавторами.
- Введение циметидина (фамотидина, кваматела, гистодила) в/в.
- Гепарин – 200 – 300 ЕД/кг в сутки в/в перфузором.
- Дезагреганты: трентал до 1000 мг, ГЭК 130.
- Нестероидные противовоспалительные средства: аспирин 200 мг/сут или аспизол 500 мг/сут.
- Инфузионная терапия: общий объём 30-35 мл/кг под контролем ЦГ и диуреза.
- При нестабильности гемодинамики вазопрессоры в соответствии с гемодинамическим портретом пациентки.
Дальнейшая тактика должна включать:
- Уход за верхними дыхательными путями (ингаляции, удаление мокроты, лечебные фибробронхоскопии – ежедневно).
- При продолжении ИВЛ более 3 суток – трахеостомия.
- Посев из трахеи и крови.
- Стимуляция моторики ЖКТ.
- Зондовое питание.
- Эластическое бинтование нижних конечностей.
- Лечебная гимнастика.
Какие же сценарии наиболее типичны для акушерского анестезиолога-реаниматолога при развитии аспирационного синдрома? Нам импонирует точка зрения А.П. Зильбера и Е.М. Шифмана:
- Если аспирация произошла на этапе индукции в наркоз, и удается уменьшить явления гипоксии и бронхиальной обструкции операцию следует начинать после выполнения всего комплекса лечебных мероприятий (санационной бронхоскопии, оптимизации вентиляции, введения бронхолитиков и т.д.).
- Если критически нарастает степень гипоксии, лечебные мероприятия неэффективны – показано экстренное абдоминальное родоразрешение в интересах плода.
- Если аспирация произошла в процессе выполнения кесарева сечения, необходима операционная пауза, за время которой анестезиолог выполнит весь комплекс мер, направленных на уменьшение гипоксии, бронхиальной обструкции.
Профилактика аспирационного синдрома
- Эвакуация зондом желудочного содержимого.
- Антациды (ранитидин, контролок, омез).
- В премедикацию включается метоклопрамид (10-20 мг)
- Если вмешательство должно начаться немедленно 0,3М р-р цитрата натрия – 30 мл дают выпить при поступлении пациентки в операционную.
При плановых операциях:
- Циметидин 400 мг на ночь и 400 мг за 2 часа до анестезии per os.
- Ранитидин 150 мг на ночь и 150 мг за 2 часа до анестезии per os.
- Омепразол 40мг на ночь и 40 мг за 2 часа до анестезии per os.
- Метоклопрамид 10 мг в/в на этапе премедикации.
При экстренных вмешательствах:
- Crush-индукция с выполнением приема Селика (давление с силой 5 кг принято в качестве золотого стандарта для взрослых) начинается сразу после преоксигенации 100% кислородом до введения мышечных релаксантов и заканчивается после интубации трахеи и раздувания манжетки.
- Если при интубации отмечается поступление желудочного содержимого в глотку немедленно придать положение Тределенбурга, которое следует соблюдать (естественно, в случае аспирации) до окончания санации трахеобронхиального дерева. Затем необходимо ввести интубационную трубку в пищевод и раздуть манжетку. После санации ротоглотки – интубация трахеи запасной интубационной трубкой, после чего ввести зонд в желудок.
Резюмируя вышесказанное, хотелось бы привести здесь одно из наших клинических наблюдений.
Пациентка Н., 28 лет, с диагнозом I срочные роды в 38-39 недель, ЭКО, умеренно выраженная преэклампсия. 10.09.2014 взята на плановую лапаротомию по Пфанненштилю. При предоперационном осмотре анестезиолога обращало на себя внимание:
- Отягощенный аллергологический анамнез – отек Квинке на антибиотики пенициллинового ряда.
- Степень сложности интубации – класс II по Mallampati.
- Анестезиологический риск по ASA II-III.
- Синдром нижней полой вены +++.
- Категорический отказ от регионарной анестезии.
На этапе индукции в анестезию молодым специалистом (2 попытки интубации трахеи) у пациентки развилась регургитация с последующей аспирацией желудочного содержимого. Пришедшим на выручку опытным анестезиологом больной немедленно было придано положение Тределенбурга, которое соблюдалось до окончания санации трахеобронхиального дерева.
Затем интубационная трубка была введена в пищевод и раздута манжетка. После санации ротоглотки – произведена интубация трахеи запасной интубационной трубкой.
Начат лаваж легких охлажденным (до 10-15° С) физиологическим раствором 10-15 мл через интубационную трубку до полного очищения. Качество лаважа (естественно, и прочих мероприятий) оказалось столь высоким, что произведенная через 30 минут экстренная бронхоскопия впервые за долгие годы наших наблюдений не выявила патологии со стороны трахеобронхиального дерева. Тем не менее, было произведено локальное введение кортикостероидов и тиенама.
Оперативность действий лечащих врачей была столь высока, что, несмотря на явные признаки аспирации (содержимое желудка в трахее, кратковременный цианоз, тахикардия, появление многочисленных хрипов в легких, повышение сопротивления вдоху до 35 см водн. ст., снижение SaO2 до 89%), в течении 10 минут была ликвидирована бронхиальная обструкция, начато кесарево сечение, а через 5 минут после начала операции извлечена живая доношенная девочка с оценкой по шкале Apgar 8-9 баллов.
В соответствии с принятым у нас стандартом, была налажена ингаляция севорана, протективная ИВЛ c РЕЕР + 8-9 см. Также назначались: бронхолитики (бриканил капельно 1,0 мг/сутки перфузором, эуфиллин 480 мг/сутки); деэскалационная антибактериальная терапия (тиенам 3 гр/сутки в/в); метилпреднизолон (3 г/сутки); НМГ и реологически активные средства, муколитики в стандартных дозировках.
Уже через 2 часа по окончанию операции через режим pressure support, после пробы на адекватность газообмена и стабильной гемодинамике переведена на спонтанное дыхание. В дальнейшем течение послеоперационного периода без особенностей, рентгенографический контроль ни в день аспирации, ни в последующие сутки патологии со стороны легких не выявил.
В.Я. Вартанов, Н.Н. Хуторская, И.Г. Труханова, Л.В. Кругова,
С.А. Василькин, Ю.Г. Кутырева, М.М. Дорожкина
2015 г.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 3 декабря 2019;
проверки требуют 3 правки.
Аспирацио́нная пневмони́я (лат. aspirātiō — «вдыхание») — воспаление лёгких, возникающее при вдыхании или пассивном попадании в лёгкие различных веществ в массивном объёме, чаще всего в практике — рвотных масс. Воспаление возникает через специфические свойства субстанций, вызывающих сильные воспалительные реакции.
К аспирационной пневмонии часто приводит регургитация (затекание) желудочного содержимого в дыхательные пути при кардиопульмональной реанимации, шоке, нарушениях сознания (в том числе, алкогольной и героиновой интоксикации), при нарушении глотания в рамках различных неврологических заболеваний (бульбарный паралич, псевдобульбарный, миастения, постравматическая энцефалопатия, тяжело протекающие нейродегенеративные заболевания, ассоциированные с нарушением нервно мышечной проводимости, запущенные менингиты, миастении дисфагии), заболеваний пищевода (ГЭРБ, рак пищевода, грыжа пищеводного отверстия и диафрагмы), тяжело протекающие уремические энцефалопатии, диабетические полиневриты. Соляная кислота содержимого желудка с низким pH (<2,5) является очень агрессивной по отношению к эпителию дыхательных путей, вызывая химический пневмонит. Данный тип поражения приводит к спазму бронхов, ателектазам, бронхоэктазам, абцессам, гангренам легких, буллюсу, альвеолиту, стридору, нарушая барьер слизистой и открывая «ворота» для инфекций. Отдельно выделяют синдром Мендельсона — аспирационную пневмонию, вызванную аспирацией желудочного содержимого у больных под наркозом[1]. Данный синдром может осложниться отеком легких и сердечно-лёгочной недостаточностью.
Лечение[править | править код]
Все случаи аспирационных процессов требуют неотложной медицинской помощи, в первых мероприятиях могут проводиться удары надбрюшной области (прием Хеймлиха) для стимуляции кашлевого рефлекса. Могут (изредка) также быть использованы аналептики. Часто показана реанимационные мероприятия в пульмонологии, отоларингологии, либо в гнойно-септическом, либо в гангренозно-некротическом отделениях торакальной хирургии, в зависимости от степени (порядок расположен от начала пневмонии по степени нарастания возможных осложнений) аспирации, важно также уточнить генез патологии, особенно при связях с неврологическими, нейродегенеративными и нейроинфекционными патологиями и процессами (в том числе и хроническими), при связях с судебной медициной, с травматологией и онкологией и токсикологией, при заболеваниях с нарушениями обмена, в каждом из случаев лечение должно быть в комплексе с основной патологией (особенно в случае бас, болезни паркинсона, ботулизма, миастении, бешенства столбняка, дифтерии, при энцефалопатиях полинейропатиях и миопатиях уремического, диабетического, токсического (отравление ФОС, полиэтиленгликолем, двуокисью углерода, фенотизианами, тирэтилсвинцом) и посттравматического генеза, и при установленных связях с нейроинфекциями), и подбираться строго индивидуально, в зависимости от первоначальной причины, в комплексе с основной патологией. Лечение в данных случаях должно быть направлено на устранение/коррекцию первопричины.
В качестве общих мер проводятся эндоскопические (чаще всего прямыми жесткими ларингоскопами, или бронхоскопами, реже эзофагоскопами) санационные мероприятия (промывание-очищение), с подключенными аспираторами, направленные на быстрое диагностирование причины и её устранение, внутривенное, эндотрахеальное, эндобронхиальное и ингаляционное вливание бронхолитиков (аминофилин), муколитиков (ацетилцистеин, бромгексин), антибиотиков (сульфамиламиды, тетрациклины, пеницилины, линкозамиды, карбапенемы, нитрофураны, цифалоспорины), противомикробных средств (тинидазол, метронидазол, орнидазол), коркистероидов (бекламетазон, бетаметазон), протеолитических ферментов (трипсин, химотрипсин, химопин и др.), антигипоксантов (актовегин, убихинон, цитохром С, натрия оксибурат, карнитин), иногда (очень редко) и диуретиков (лазикс, манитол), витаминов групп А, Е и B, метаболические средства, в некоторых случаях может проводиться также трахеостомия торакоэктомия. Могут применяться системные антигипоксанты (цитохром, карбоксилаза, триметазидин, натрия оксибурат), а также адренометики (астмопент, беродуал).
Примечания[править | править код]
Источник
Под бронхообструктивным синдромом (БС) понимают совокупность клинических симптомов, отражающих нарушение проходимости бронхов вследствие сужения их просвета. БС нередко встречается у детей раннего возраста. От 30 до 50% детей первых трех лет жизни имеют те или иные проявления бронхообструктивного синдрома, вследствие чего проблемы дифференциальной диагностики этого состояния крайне важны.
БС — это ведущий признак, который объединяет группу острых, рецидивирующих и хронических заболеваний легких, но он не является самостоятельной нозологической формой и не может фигурировать в качестве диагноза. Следует отметить, что БС не синоним бронхоспазма, хотя во многих случаях бронхоспазм играет важную, а иногда ведущую роль в генезе заболевания. Обычно БС выявляется у детей первых четырех лет жизни, но может диагностироваться и в более старшем возрасте.
В таблице 1 указаны основные причины возникновения БС у детей.
Наиболее важное значение имеют возрастные особенности респираторной системы ребенка. Бронхи у маленьких детей имеют меньший диаметр, чем у взрослых. Слизистая трахеи и бронхов быстро реагирует отеком и гиперсекрецией слизи в ответ на развитие вирусной инфекции. Узость бронхов и всего дыхательного аппарата значительно увеличивает аэродинамическое сопротивление. Так, отек слизистой бронхов всего на 1 мм вызывает повышение сопротивления току воздуха в трахее более чем на 50% [1].
Для детей раннего возраста характерны податливость хрящей бронхиального тракта, недостаточная ригидность костной структуры грудной клетки, свободно реагирующей втяжением уступчивых мест на повышение сопротивления в воздухоносных путях, а также ряд особенностей положения и строения диафрагмы. Несомненное влияние на функциональные нарушения органов дыхания у маленького ребенка оказывают и такие факторы, как более длительный сон, частый плач, преимущественное положение лежа на спине в первые месяцы жизни.
Важную роль играет респираторная вирусная инфекция. К числу вирусов, наиболее часто вызывающих БС, относят респираторно-синцитиальный вирус (около 50%), вирус парагриппа, микоплазму пневмонии, реже — вирусы гриппа и аденовирус.
Среди факторов окружающей среды, которые могут приводить к развитию обструктивного синдрома, особо важное значение придается пассивному курению в семье. Под влиянием табачного дыма происходит гипертрофия бронхиальных слизистых желез, нарушается мукоцилиарный клиренс, замедляется продвижение слизи. Пассивное курение провоцирует деструкцию эпителия бронхов. Особенно ранимыми в этом плане считаются дети первого года жизни.
Другим важным неблагоприятным фактором является загрязнение окружающей атмосферы индустриальными газами, а также органической и неорганической пылью.
Большинство исследователей признают влияние факторов преморбидного фона на развитие БС. Это — токсикозы беременных, осложненные роды, гипоксия в родах, недоношенность, отягощенный аллергологический анамнез, гиперреактивность бронхов, рахит, дистрофия, гиперплазия тимуса, перинатальная энцефалопатия, раннее искусственное вскармливание, перенесенное респираторное заболевание в возрасте 6—12 месяцев.
В таблице 2 представлены основные нозологические формы, при которых бронхообструктивный синдром может иметь место и в значительной степени определять клиническую симптоматику болезни.
Бронхиальная астма представляет собой заболевание, проявляющееся обратимой (полностью или частично) обструкцией бронхов, патогенетическую основу которого составляют аллергическое воспаление дыхательных путей и, в большинстве случаев, гиперреактивность бронхов. Оно характеризуется в типичных случаях периодическим возникновением приступов нарушения проходимости бронхов в результате их спазма, отека слизистой оболочки бронхов и гиперсекреции слизи.
Бронхиальная астма может протекать также в виде астматического бронхита без типичных приступов, спастического кашля (в том числе ночного), астмы физического напряжения.
Критерии диагностики: приступы удушья, астматический статус, астматический бронхит, приступы спастического кашля, сопровождающиеся острым вздутием легких и затруднением выдоха. Рентгенологически во время приступа обычно определяется вздутие легких, на фоне которого нередко выявляется усиление бронхососудистого рисунка.
Под обструктивным бронхитом понимают острое поражение бронхов, сопровождающееся клиническими признаками бронхиальной обструкции. Термин «бронхиолит» используется для обозначения тех форм обструктивного бронхита, которые сопровождаются большим количеством рассеянных мелкопузырчатых хрипов, что нередко наблюдается у детей первых месяцев жизни при первом эпизоде обструктивного заболевания.
Наибольшие сложности представляет дифференциальная диагностика обструктивного бронхита и бронхиальной астмы.
До 70-х г. прошлого века термин «обструктивный бронхит» и его аналоги (астматический бронхит, спастический бронхит и др.) широко использовались педиатрами. Однако в начале 70-х гг. была проведена серия эпидемиологических исследований, которые показали, что отличить обструктивный бронхит и бронхиальную астму в широкой педиатрической практике почти невозможно. Таким образом, был поставлен знак равенства между этими состояниями. Данный подход у детей старшего возраста в значительной степени себя оправдал, так как позволил избавить многих больных от антибактериальной терапии. Но у детей младшего возраста проблема стоит сложнее. Выяснилось, что кромогликат у этих больных недостаточно эффективен или неэффективен вовсе. Ингаляционные бронходилятаторы, такие, как сальбутамол, малоэффективны или не эффективны при свистящем дыхании у детей первых трех лет жизни. Сведения относительно действенности применения ингаляционных стероидов при остром или хроническом бронхиолите оказались противоречивыми.
К тому же многочисленные исследования в нашей стране и за рубежом показали, что исходы обструктивного бронхита в целом благоприятны. 54% детей с повторными эпизодами обструктивного бронхита перестают болеть после четырех лет, а еще 37% — в более позднем возрасте; таким образом, выздоравливают более 90% пациентов. Кроме того, наличие обструктивного синдрома в первые три года жизни не может рассматриваться как фактор, предрасполагающий к возникновению астмы в дальнейшем. Т. е. выяснилось, что механизм развития свистящего дыхания у детей раннего возраста другой, чем у более старших детей, и основную роль здесь играют не гиперреактивность слизистой бронхов и спазм мышц, а тонус бронхиальной стенки и отек слизистой бронхов. Это отражало тот факт, что «свистящее дыхание» у маленьких детей является следствием различных причин, в том числе аномалий респираторной системы и воспалительных процессов иной этиологии.
Значит ли это, что у малышей не бывает астмы? По-видимому, нет, так как примерно у 10% больных, у которых на фоне вирусной инфекции отмечался БС, в дальнейшем могли развиваться симптомы астмы. Рецидивы обструкции обусловлены наследственной отягощенностью по аллергии и аллергическими реакциями у ребенка и не связаны с кожными тестами и уровнем IgE. Таким образом, можно утверждать, что обструктивный бронхит, как нозологическая форма, существует. Его основные отличия от астмы представлены в таблице 3.
| Таблица 3. Дифференциальная диагностика бронхиальной астмы и обструктивного бронхита. |
Дифференциальную диагностику обструктивного бронхита и острой пневмонии облегчает тот факт, что при пневмонии, вызванной основными возбудителями, как правило, не наблюдается обструкции. Сопровождаться обструкцией могут, в основном, внутрибольничные пневмонии, обусловленные некоторыми грамотрицательными возбудителями кишечной группы (см. таблицу 4).
| Таблица 4. Дифференциальная диагностика обструктивного бронхита и острой пневмонии. |
Аспирационный синдром
Одна из наиболее распространенных причин развития БС у грудных детей — синдром привычной микроаспирации жидкой пищи, связанный с дисфагией, часто в сочетании с желудочно-пищеводным рефлюксом. До 30% всех случаев рецидивирующего кашля у детей раннего возраста связаны с аспирационным синдромом. Выяснить причину бывает сложно. В диагностике аспирации помогают данные анамнеза, обычно у этих детей имеется отягощенный неврологический анамнез и такие признаки, как приступообразный кашель, развивающийся у ребенка во время кормления, появление сухих или влажных хрипов в легких после еды. Подтверждается диагноз при обследовании в стационаре.
Аспирация инородных тел
До 50% всех аспираций инородных тел вовремя не выявляется. Поздняя диагностика связана с тем, что после аспирации у ребенка на фоне полного здоровья, без катаральных явлений, возникает острый приступ кашля, затем, если инородное тело проникает глубже, через несколько дней появляются симптомы обструктивного бронхита или пневмонии с обструктивным синдромом, имеющих затяжное, трудно поддающееся терапии течение.
В диагностике помогают анамнез, рентгенологическое исследование и бронхоскопия.
Хронический бронхит
Критерии диагностики: продуктивный кашель, постоянные разнокалиберные влажные хрипы в легких (в течение нескольких месяцев) при наличии двух-трех обострений заболеваний в год на протяжении двух лет.
У взрослых основные причины ХБ — это курение и профессиональные вредности. Причем у половины больных это заболевание протекает с признаками бронхообструктивного синдрома. В детском возрасте первичный хронический бронхит — большая редкость. В большинстве случаев он является следствием других причин (пороков развития легких, иммунодефицитных состояний и др.), т. е. является «вторичным». Поэтому диагноз «первичный хронический бронхит» может ставиться только после тщательной дифференциальной диагностики.
Хроническая пневмония
Хроническая пневмония представляет собой хронический воспалительный неспецифический процесс, имеющий в своей основе необратимые морфологические изменения в виде деформации бронхов и пневмосклероза в одном или нескольких сегментах и сопровождающийся рецидивами воспаления в бронхах и легочной ткани. Хроническая пневмония чаще всего развивается как результат неполного излечения острой пневмонии, ателектаза, а также вследствие попадания инородного тела в бронхи.
Особенностью этого заболевания в настоящее время является его благоприятное течение и высокая частота сопутствующего бронхообструктивного синдрома (30—35%). Диагностика этой болезни основывается на клинической симптоматике, рентгенологических и бронхологических данных и осуществляется в специализированном стационаре.
Хронический бронхиолит с облитерацией
Заболевание, развивающееся вследствие острого облитерирующего бронхиолита, морфологическим субстратом которого является облитерация бронхиол и артериол одного или нескольких участков легких, приводящая к нарушению легочного кровотока и развитию эмфиземы. Синдром одностороннего сверхпрозрачного легкого (синдром МакЛеода) представляет собой частный случай данного заболевания.
Клинически проявляется одышкой и другими признаками дыхательной недостаточности разной степени выраженности, локальными физикальными данными в виде стойкой крепитации и мелкопузырчатых хрипов. У детей старшего возраста может сопровождаться бронхообструктивным синдромом, имеющим торпидное, плохо поддающееся лечению бронходилятаторами течение.
При наличии клинических данных и рентгенологических признаков сверхпрозрачности сцинтиграфически определяется резкое снижение легочного кровотока в пораженных отделах легких.
Синдром цилиарной дискинезии
Заболевание проявляется рецидивирующими синуситами и отитами и хроническим поражением легких — это хронический бронхит с образованием бронхоэктазов. Типичное проявление этой болезни — синдром Картагенера, когда у пациента имеет место еще и обратное расположение внутренних органов. В основе синдрома лежит врожденный дефект цилиарного эпителия, приводящий к дисфункции мукоцилиарного транспорта и застою секрета в бронхах. Почти у всех больных могут отмечаться эпизоды приступообразного кашля, одышки.
Дифференциальная диагностика основывается на обратном расположении внутренних органов, рентгенологических данных и исследовании функции цилиарного эпителия.
Врожденные пороки развития бронхов
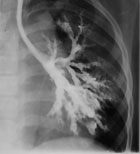 |
| Рисунок 1. Бронхограмма левого легкого ребенка с синдромом Вильямса-Кемпбелла. |
Из этой многочисленной группы заболеваний наибольший интерес представляют пороки развития трахеи и бронхов. Недоразвитие хрящей трахеи и или бронхов приводит к тому, что бронхи спадаются на выдохе, обуславливая поведение симптоматики БС. Первые клинические проявления заболевания возникают на первом году жизни — это либо повторные обструктивные бронхиты, либо пневмонии. В дальнейшем формируется деформация грудной клетки, появляется влажный постоянный кашель, выслушиваются влажные и сухие хрипы в легких. Диагноз обычно ставится в младшем или старшем школьном возрасте, когда клиническая симптоматика ярко выражена. В дифференциальной диагностике, наряду с клинической симптоматикой, важны рентгенологическое исследование и бронхоскопия, а также резистентность к бронходилятаторам и высокая эффективность антибактериальной терапии. На рисунке показана бронхограмма больного с недоразвитием хрящей бронхов 3—8 генерации (синдром Вильямса-Кемпбелла). Хорошо видно чрезмерное расширение бронхов в зоне поражения.
Стенозы трахеи и бронхов — это состояние, встречающееся достаточно редко. Их отличает постоянное шумное дыхание у ребенка и на вдохе и на выдохе, усиливающееся при присоединении ОРВИ. Диагноз подтверждается при рентгенологическом и бронхологическом обследовании.
Опухоли трахеи и бронхов у детей также диагностируются нечасто. Опухоли могут приводить к сужению просвета дыхательных путей как при сдавлении извне, так и при прорастании внутрь просвета. Помочь в диагностике может постепенное нарастание синдрома «шумного дыхания», которое вначале появляется при ОРВИ, а затем и в состоянии покоя.
Диагноз подтверждается при рентгенологическом и бронхологическом обследовании.
Муковисцидоз
Муковисцидоз (МВ) — генетическое, аутосомно-рецессивное моногенное заболевание, обусловленное мутацией гена трансмембранного регулятора МВ (МВТР). Характеризуется нарушением секреции экзокринных желез жизненно важных органов с поражением, прежде всего, дыхательного и желудочно-кишечного трактов, тяжелым течением и неблагоприятным прогнозом. Особенность клинических проявлений болезни заключается в приступообразном коклюшеподобном кашле с вязкой мокротой, вследствие чего иногда путают с бронхиальной астмой.
Дифференциальная диагностика: наличие кишечного синдрома (нейтральный жир в стуле), прогрессирующая дыхательная недостаточность, изменения на рентгенограммах и положительный потовый тест.
Бронхолегочная дисплазия
Хроническое заболевание, развивающееся вследствие поражения легких при проведении жестких режимов искусственной вентиляции легких с высокими концентрациями кислорода, главным образом у недоношенных детей. В основе заболевания лежат нарушение архитектоники легочной ткани и, часто, бронхиальная гиперреактивность. Клинически проявляется гипоксемией, дыхательной недостаточностью, симптомами бронхиальной обструкции; рентгенологически обычно выявляются грубые изменения в виде фиброза, кист, изменений прозрачности легочной ткани, деформаций бронхов. Диагностика осуществляется на основании анамнестических, клинических и рентгенологических данных.
Внелегочные причины БС диагностируются при обследовании больного в стационаре.
Таким образом, БС нередко сопровождает легочные и внелегочные патологические процессы. Дифференциальная диагностика при этих состояниях включает ряд нозологических форм. При затяжном течении БС, а также при повторных эпизодах обструкции больной должен быть обследован в специализированном пульмонологическом стационаре и наблюдаться там в дальнейшем.
Обратите внимание!
- От 30 до 50% детей первых трех лет жизни имеют те или иные проявления бронхообструктивного синдрома.
- числу вирусов, наиболее часто вызывающих БС, относят респираторно-синцитиальный вирус, вирус парагриппа, микоплазму пневмонии, реже — вирусы гриппа и аденовирус.
- Наибольшие сложности представляет дифференциальная диагностика обструктивного бронхита и бронхиальной астмы.
И. К. Волков, доктор медицинских наук
Отд. пульмонологии НИИ педиатрии
