Антифосфолипидный синдром код мкб
Содержание
- Описание
- Симптомы
- Дифференциальная диагностика
- Причины
- Лечение
Названия
Антифосфолипидный синдром.

Антифосфолипидный синдром
Описание
Антифосфолипидный синдром — симптомокомплекс, в основе которого лежит развитие аутоиммунной реакции и появление антител к широко распространенным фосфолипидным детерминантам, присутствующим на мембранах тромбоцитов, клеток эндотелия, нервной ткани.
Антифосфолипидный синдром впервые был детально описан при системной красной волчанке Hughes.
Существует несколько классов мембранных фосфолипидов, различающихся по структуре и иммуногенности. Наиболее распространены в организме «нейтральные» фосфолипиды — фосфатидилэтаноламин (ФЭ) и фосфатидилхолин (ФХ). «Отрицательно заряженные» (анионные) фосфолипиды — фосфатидилсерин (ФС), фосфатидилинозитол (ФИ) и кардиолипин (дифосфатидилглицерол) локализуются на внутренней поверхности биомембран и экспонируются в процессе клеточной активации.
Антитела к фосфолипидам — это гетерогенная популяция антител, реагирующих с отрицательно заряженными, реже — нейтральными фосфолипидами. К антифосфолипидным антителам относятся следующие разновидности антител:
*волчаночный антикоагулянт — популяция антифосфолипидных антител класса IgG или IgM, способных in vitro подавлять фосфолипиднозависимые коагуляционные реакции путем взаимодействия с фосфолипидным компонентом протромбиназы активаторного комплекса. Волчаночный антикоагулянт был обнаружен вначале в сыворотке крови больных системной красной волчанкой. При системной красной волчанке продукция волчаночного антикоагулянта ассоциируется, в отличие от результатов in vitro, не с кровоточивостью, а с парадоксальным увеличением частоты тромбозов;
*антитела к кардиолипину — иммунологически гетерогенная популяция антител, реагирующих с иммобилизованным отрицательно заряженным фосфолипидом — кардиолипином, являющимся основным антигеном реакции Вассермана; антитела к кардиолипину могут относится к различным изотипам иммуноглобулинов IgG, IgM, IgA;
*антитела, реагирующие со смесью кардиолипина, холестерина, фосфатидилхолина, определяемые с помощью реакции агглютинации (ложноположительная реакция Вассермана);
*бета2-гликопротеин-1-кофакторзависимые антифосфолипидные антитела (бета2-ГП1-кофакторзависимые АФЛ) — подавляющие естественную антикоагулянтную активность бета2-ГП1. При антифосфолипидном синдроме взаимодействие АФЛ с фосфолипидами зависит от кофактора бета2-гликопротеина-1. Он имеет молекулярную массу 50,000,000 Да и активно связывается с фосфолипидами, ДНК, компонентами мембран тромбоцитов и митохондрий, гепарином. Бета2-ГП1 является важным естественным антикоагулянтом, он подавляет внутреннюю активацию антикоагуляционного каскада и агрегацию тромбоцитов. Подавление бета2-ГП1-кофакторзависимых антител сопровождается развитием тромбозов.
Частота обнаружения антител к фофолипидам в сыворотке крови здоровых людей колеблется от 1 до 12% и может увеличиваться у лиц пожилого возраста.
В сыворотке здоровых людей уровень антител к фосфолипидам низкий, при этом биологические мембраны защищены от воздействия последних.
При заболеваниях, связанных с активацией В-лимфоцитов, резко увеличивается концентрация антител к фосфолипидам. Наиболее часто и в высоком титре антител к фосфолипидам обнаруживаются в сыворотке крови больных системной красной волчанкой (до 70% случаев), реже — при других ревматических заболеваниях, включая ревматоидный артрит, системную склеродермию, синдром Шегрена. Избыточное образование антител к фосфолипидам выявлено также у больных со злокачественными новообразованиями, лимфопролиферативными синдромами, аутоиммунной тромбоцитопенической пурпурой, на фоне острых и хронических вирусных, бактериальных и паразитарных инфекций (инфекционный мононуклеоз, СПИД и ), при ряде заболеваний ЦНС, некоторых формах акушерской патологии, на фоне приема некоторых широко распространенных лекарственных препаратов (оральных контрацептивов, психотропных средств и ). Как правило, гиперпродукция антител к фосфолипидам приводит к развитию антифосфолипидного синдрома.
Антифосфолипидный синдром чаще встречается у женщин, чем у мужчин.
Симптомы
Венозный и артериальный тромбоз.
Наиболее характерен рецидивирующий венозный тромбоз. Тромбы обычно локализуются в глубоких венах нижних конечностей, нередко в почечных и печеночных венах, приводя к развитию нефротического синдрома и синдрома Бадда-Киари. Часто наблюдаются эмболии из глубоких вен нижних конечностей в легочную артерию, капилляриты, что приводит к развитию легочной гипертензии и легочным геморрагиям. Описаны тромбозы подключичной вены, вены сетчатки. Возможно развитие синдрома верхней или нижней полой вены при тромбозе соответствующей локализации. Тромбоз центральной вены надпочечников с последующим развитием геморрагии и их некроза приводит к развитию хронической надпочечниковой недостаточности.
Артериальный тромбоз клинически проявляется ишемией и гангреной нижних конечностей, синдромом дуги аорты, асептическим некрозом головки бедра. Тромбозы обусловлены взаимодействием антифосфолипидных антител с эндотелиальными клетками и снижением антитромботической активности эндотелия, подавлением продукции простациклина и повышением агрегации тромбоцитов, снижением активности циркулирующих антикоагулянтных факторов (антитромбина III, белка С и S, бета2-ГП1 и ).
Поражение ЦНС.
Тромбоз артерий головного мозга приводит к транзиторным ишемическим атакам, рецидивирующим инсультам, которые могут проявиться не только парезами и параличами, но и судорожным синдромом, прогрессирующим слабоумием, психическими нарушениями. Возможны и другие неврологические нарушения: мигренеподобные головные боли, хорея, поперечный миелит. Не исключено, что синдром Снеддона (сочетание сетчатого ливедо, рецидивирующего тромбоза церебральных артерий и артериальной гипертензии) также является проявлением антифосфолипидного синдрома.
Поражение сердца.
Кардиальная патология может иметь серьезное прогностическое значение и следующие клинические проявления:
- тромбоз коронарных артерий и развитие инфаркта миокарда;
- острый или хронический тромбоз мелких интрамуральных ветвей коронарных артерий, что приводит к нарушению сократительной способности миокарда;
-поражение клапанов сердца (недостаточность митрального клапана или сужение левого атриовентрикулярного отверстия, реже — недостаточность аортального или трикуспидального клапанов).
-возможно формирование внутрипредсердных тромбов, что на поминает клинические проявления миксомы сердца;
- часто развивается артериальная гипертензия лабильная или стабильная, которая обусловлена тромбозом почечных сосудов, инфарктом почек, тромбозом брюшного отдела аорты, интрагломерулярным тромбозом почек, развитием фибромышечной дисплазии почечных артерий.
Поражение почек.
При антифосфолипидном синдроме нередко наблюдается тромбоз почечной артерии, инфаркт почки, а также внутриклубочковый микротромбоз («почечная тромботическая микроангиопатия») с последующим развитием гломерулосклероза и хронической почечной недостаточности.
Поражение печени.
Возможен тромбоз печеночных вен (синдром Бадда-Киари), поражение артерий с развитием инфаркта печени, развитие узловой регенераторной гиперплазии.
Поражение легких.
Возможны тромбоэмболии легочной артерии и реже — тромботическая легочная гипертензия, обусловленная местным тромбозом легочных сосудов.
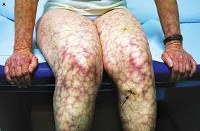
Поражение кожи.
Кожными проявлениями антифосфолипидного синдрома являются сетчатое ливедо (сосудистая сеточка в виде синеватых пятен на голенях, ступнях, бедрах, кистях, особенно хорошо выявляемая при охлаждении); поверхностная сыпь в виде точечных геморрагии, напоминающих васкулит; некроз кожи дистальных отделов нижних конечностей; хронические язвы ног; кровоизлияния в подногтевое ложе (симптом «занозы»).
Акушерская патология.
Является наиболее характерным проявлением антифосфолипидного синдрома. Возможны следующие виды акушерской патологии: привычное невынашивание беременности, рецидивирующие спонтанные аборты (риск выкидышей увеличивается с увеличением концентрации антикардиолипина класса IgG), внутриутробная гибель плода, поздний токсикоз беременности, преэклампсия, эклампсия, хорея, задержка внутриутробного развития плода, преждевременные роды. Основными механизмами акушерской патологии являются: тромбоз сосудов плаценты, развитие инфаркта и недостаточности плаценты, угнетение синтеза простациклина, дефицит которого обусловливает гипертонус матки и выкидыш.
Судороги.
Антифосфолипидный синдром
Дифференциальная диагностика
У некоторых больных возможно развитие тромботических наслоений на клапанах (вегетации), что трудно дифференцировать от инфекционного эндокардита;
Причины
Антифосфолипидный синдром может быть первичным, не связанным с какой либо предшествующей патологией, но наиболее часто развивается при названных выше заболеваниях, сопровождающихся продукцией антифосфолипидных антител. Существует генетическая предрасположенность к гиперпродукции антител к фосфолипидам, которая связана с носительством антигенов HLA DR7, DQBj, DR4, а также нулевого аллеля Сф. Основным патогенетическим механизмом антифосфолипидного синдрома является влияние антифосфолипидных антител на сосудистые, клеточные и гуморальные компоненты системы коагуляции, что приводит к нарушению равновесия между протромботическими и антитромботическими процессами и развитию тромбозов.
Антифосфолипидные антитела оказывают следующие патогенетические влияния:
*эндотелиальная клетка: снижение синтеза простациклина — простагландина, обладающего антиагрегационным и вазодилатирующим эффектом; нарушение функциональной активности тромбомодулина — белка, содержащегося на поверхности эндотелия, прямо тормозящего прокоагулянтную активность тромбина и ускоряющего активацию протеина С тромбином; снижение активности гепаран-сульфата; индуцирование образования фактора активации тромбоцитов; нарушение фибринолитической активности; снижение высвобождения тканевого активатора плазминогена; увеличение высвобождения ингибитора активатора плазминогена 1; увеличение синтеза фактора Виллебранда, необходимого для нормальной агрегации тромбоцитов и обладающего способностью удлинять период полувыведения фактора VIII;
*тромбоциты: антифосфолипидные антитела взаимодействуют с тромбоцитами, вызывают увеличение продукции тромбоксана Аг, концентрации цитозольного кальция, что ведет к увеличению агрегации тромбоцитов; кроме того, антифосфолипидные антитела связываются с мембраной активированных тромбоцитов, что вызывает более быстрое разрушение их фагоцитирующими мононуклеарами, в результате чего развивается тромбоцитопения;
*гуморальные компоненты коагуляции: снижение активации белка С и уровня свободного белка S — в норме активированный протеин С в присутствии своего кофактора белка S избирательно разрушает факторы Va и VIIIa, что способствует угнетению свертывания крови; ослабление активности гепарина и гепаринопосредованного образования комплекса антитромбин III-гепарин; снижение синтеза и функциональной активности плацентарного антикоагулянта; нарушение функциональной активности естественного антикоагулянта бета2-ГП1.
Лечение
Профилактика и лечение тромбозов при АФС — не менее сложная задача, чем его корректная диагностика. Это связано с неоднородностью патогенетических механизмов, лежащих в основе АФС, полиморфизмом клинических проявлений, отсутствием достоверных клинических и лабораторных показателей, позволяющих прогнозировать рецидивирование тромботических нарушений. Фактически до сих пор не разработаны общепринятые на международном уровне стандарты, касающиеся тактики ведения пациентов с различными формами АФС, а предлагаемые в настоящее время рекомендации основаны на результатах открытых испытаний или ретроспективного анализа исходов заболевания. Следует сразу подчеркнуть, что глюкокортикоиды (ГК), а также цитотоксические препараты и плазмоферез при АФС применяются только для подавления активности основного заболевания (например, СКВ) или при катастрофическом АФС. В остальных случаях они неэффективны (и даже противопоказаны), поскольку длительная глюкокортикоидная терапия потенциально может увеличивать риск рецидивирования тромбозов, а некоторые цитотоксические препараты (и ГК) увеличивают риск развития осложнений антикоагулянтной терапии.
Очевидно, что поскольку для АФС характерен высокий риск рецидивирования тромбозов, подавляющее большинство пациентов нуждаются в проведении профилактической антикоагулянтной терапии в течение длительного времени, иногда пожизненно. Исключение могут составить пациенты со стойкой (в течение нескольких лет) нормализацией уровня аФЛ в отсутствие рецидивов тромбозов. Однако и в этом случае риск рецидивирования тромбозов не может быть полностью исключен, и пациенты нуждаются в тщательном динамическом наблюдении и, вероятно, приеме низких доз аспирина.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 июля 2019;
проверки требуют 2 правки.
Антифосфолипидный синдром (АФС), или фосфолипидный синдром, или синдром антифосфолипидных антител (АФС или САФА) — аутоиммунное состояние гиперкоагуляции, вызванное антифосфолипидными антителами. АФС провоцирует образование тромбов (тромбоз) как в артериях, так и венах, а также связанные с беременностью осложнения, такие как выкидыш, мертворождение, преждевременные роды и тяжелая преэклампсия.
Диагностические критерии постановки диагноза АФС требуют наличия одного клинического события, такого как тромбоз или осложнение беременности, а также проведения двух анализов крови на антитела, разнесённых по крайней мере на три месяца друг от друга, которые подтверждают наличие либо волчаночного антикоагулянта, либо анти-бета-2-гликопротеина-I.
Антифосфолипидный синдром может быть первичным или вторичным. Первичный антифосфолипидный синдром возникает в отсутствие каких-либо других связанных с ним заболеваний. Вторичный антифосфолипидный синдром встречается совместно с другими аутоиммунными заболеваниями, такими как системная красная волчанка (СКВ). В редких случаях АФС приводит к быстрой полиорганной недостаточности вследствие генерализованного тромбоза, это явление называется «катастрофическим антифосфолипидным синдромом» (или синдромом Ашерсона) и ассоциируется с высоким риском смерти.
История открытия[править | править код]
Антифосфолипидный синдром был впервые полностью описан в 1980-х годах после различных предыдущих докладов о специфических антителах у людей с системной красной волчанкой и тромбозом[2][3]. Этот синдром иногда называют «синдромом Хьюза», после того, как ревматолог Грэм Р. В. Хьюз, работавший в больнице Святого Томаса в Лондоне, подробно описал это состояние[3][4].
Симптомы[править | править код]
Наличие антифосфолипидных антител в отсутствие тромбов или связанных с беременностью осложнений не указывает на АФС. Антифосфолипидный синдром может привести к артериальным или венозным сгусткам крови в любых органах, или к связанным с беременностью осложнениям.[5] . У пациентов с АФС наиболее распространенным симптомом является тромбоз глубоких вен нижних конечностей, а также артериальный тромбоз. У беременных женщин, страдающих от АФС, существует повышенный риск повторного выкидыша, внутриутробного ограничения роста плода и преждевременных родов. Часто причиной таких осложнений является плацентарный инфаркт.
К другим общим симптомам, которые не являются частью критериев классификации АФС, относятся низкий уровень тромбоцитов, болезнь клапанов сердца и ретикулярная асфиксия[6]. Существует также взаимосвязь между антифосфолипидными антителами и головными болями, мигренями и осциллопсией. Некоторые исследования показали наличие антифосфолипидных антител в крови и спинномозговой жидкости пациентов с психологическими симптомами[7]. У очень малого количества пациентов первичный АФС приводит к развитию системной красной волчанки.
Патогенез[править | править код]
Факторы риска развития антифосфолипидного синдрома: для первичного АФС — это генетический маркер HLA-DR7, для вторичного АФС — генетические маркеры HLA-B8, HLA-DR2 и DR3-HLA, а также системная красная волчанка или другие аутоиммунные заболевания.
Антифосфолипидный синдром является аутоиммунным заболеванием, в котором антифосфолипидные антитела (антикардиолипиновые антитела и волчаночный коагулянт) взаимодействуют с белками, которые связываются с анионными фосфолипидами на плазматических мембранах. Как и многие другие аутоиммунные заболевания, этот синдром чаще встречается у женщин, чем у мужчин. Точная причина заболевания неизвестна, но очевидно, что происходит активация системы свёртывания крови. Клинически важные антифосфолипидные антитела (те, которые возникают в результате аутоиммунного процесса) связаны с тромбозом и сосудистыми заболеваниями[8].
Лечение[править | править код]
Часто это заболевание лечится аспирином (реже варфарином), который ингибирует активацию тромбоцитов и выступает в качестве антикоагулянта. Цель профилактического лечения варфарином — поддержание МНО пациента между 2,0 и 3,0. Обычно антикоагулянты не назначаются пациентам, которые не имели тромботических симптомов. Во время беременности вместо варфарина (который может проникать через плаценту и обладает тератогенным действием) обычно применяют гепарин с низким молекулярным весом и низкие дозы аспирина. В трудноизлечимых случаях пациенту может быть назначен иммуноглобулин, а также плазмаферез[9][10].
Прогноз[править | править код]
Долгосрочный прогноз для АФС определяется в основном рецидивом тромбоза, который может возникнуть менее чем у трети больных, иногда, несмотря на антитромботическую терапию.
В популярной культуре[править | править код]
Первичный антифосфолипидный синдром становится окончательным диагнозом пациента в пятом эпизоде шестого сезона сериала «Доктор Хаус». Пациент выздоравливает.
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Ruiz-Irastorza G., Crowther M., Branch W., Khamashta M.A. Antiphospholipid syndrome (англ.) // The Lancet. — Elsevier, 2010. — October (vol. 376, no. 9751). — P. 1498—1509. — doi:10.1016/S0140-6736(10)60709-X. — PMID 20822807.
- ↑ 1 2 Hughes G.R. Thrombosis, abortion, cerebral disease, and the lupus anticoagulant (англ.) // Br. Med. J. (Clin Res Ed) : journal. — 1983. — October (vol. 287, no. 6399). — P. 1088—1089. — doi:10.1136/bmj.287.6399.1088. — PMID 6414579.
- ↑ Sanna G., D’Cruz D., Cuadrado M.J. Cerebral manifestations in the antiphospholipid (Hughes) syndrome (англ.) // Rheumatic Diseases Clinics of North America (англ.)русск. : journal. — 2006. — August (vol. 32, no. 3). — P. 465—490. — doi:10.1016/j.rdc.2006.05.010. — PMID 16880079.
- ↑ Tong M., Viall C. A., Chamley L. W. Antiphospholipid antibodies and the placenta: a systematic review of their in vitro effects and modulation by treatment (англ.) // Human Reproduction (англ.)русск. : journal. — 2014. — Vol. 21, no. 1. — P. 97—118. — doi:10.1093/humupd/dmu049. — PMID 25228006.
- ↑ Rinne T., Bronstein A.M., Rudge P., Gresty M.A., Luxon L.M. Bilateral loss of vestibular function: clinical findings in 53 patients (англ.) // Journal of Neurology (англ.)русск. : journal. — 1998. — Vol. 245, no. 6—7. — P. 314—321. — doi:10.1007/s004150050225. — PMID 9669481.
- ↑ Sokol D.K., O’Brien R.S., Wagenknecht D.R., Rao T., McIntyre J.A. Antiphospholipid antibodies in blood and cerebrospinal fluid of patients with psychosis (англ.) // Journal of Neuroimmunology (англ.)русск. : journal. — 2007. — Vol. 190, no. 1. — P. 151—156. — doi:10.1016/j.jneuroim.2007.08.002. — PMID 17868908.
- ↑ Triplett D.A. Antiphospholipid antibodies. (англ.) // Archives of Pathology & Laboratory Medicine (англ.)русск.. — 2002. — November (vol. 126, no. 11). — P. 1424—1429. — doi:10.1043/0003-9985(2002)1261424:AA2.0.CO;2. — PMID 12421152.
- ↑ de Jong P.G., Goddijn M., Middeldorp S. Antithrombotic therapy for pregnancy loss (англ.) // Human Reproduction (англ.)русск.. — 2013. — Vol. 19, no. 6. — P. 656—673. — doi:10.1093/humupd/dmt019. — PMID 23766357.
- ↑ Horton J.D., Bushwick B.M. Warfarin therapy: evolving strategies in anticoagulation (англ.) // American Family Physician (англ.)русск. : journal. — 1999. — Vol. 59, no. 3. — P. 635—646. — PMID 10029789.
Источник
