Анализы при геморрагической лихорадке с почечным синдромом
Содержание статьи:
Геморрагическая лихорадка с почечным синдромом (ГЛПС, мышиная лихорадка) – заболевание, которое вызывает контакт с выделениями грызунов. Инфицирование происходит группой вирусов, принадлежащих к роду Hantavirus семейства Bunyaviridae.
Патогенез неизвестен, но по данным исследований установлено, что иммунные механизмы играют важную роль.
Тяжелые формы ГЛПС регистрируют в странах Востока. Количество заболевших в Китае составляет примерно 100-250 тысяч в год. Мягкая форма чаще встречается в скандинавских странах Скандинавии. Заболеть ГЛПС можно в течение года, но заболеваемость зависит от динамики популяции грызунов-носителей.
Сезонные вспышки ГЛПС весной и осенью происходят из-за активного размножения мышей и связаны с увеличением контактов с грызунами на фоне садово-полевых работ. Наиболее тяжелая форма геморрагической лихорадки с синдромом почечной недостаточности вызвана вирусом Хантаан (HTNV) в Азии. Пуумала – наиболее распространенный хантавирус, но заболевание протекает легче. Встречается в Европе, России, и Балканах. Вирус Dobrava инициирует более тяжелую форму ГЛПС. Причины различий в клинической тяжести неизвестны. Смертность и заболеваемость варьируются от 5-15% в зависимости от патогенности штамма возбудителя.
Эпидемиология

Повышенная заболеваемость у мужчин обусловлена их более высокой активностью на открытом воздухе, что приводит к контакту с инфицированными грызунами.
Возраст
Геморрагическая лихорадка с синдромом почечной недостаточности обычно развивается у лиц старше 15 лет (20-60). У детей и подростков младше 15 лет болезнь является легкой и часто протекает в субклинической форме.
Причины
Вирусы рода Hantavirus (семейство Bunyaviridae) вызывают различные формы геморрагической лихорадки с синдромом почечной недостаточности. Тяжесть заболевания зависит от штамма вируса и географического распределения. Хантавирусы, связанные с ГЛПС, включают вирус Хантаан (HTNV), Добрава / Белград (DOBV), Сеул (SEOV), Пуумала (PUUV) и Сааремаа (SAAV).
• Корейская геморрагическая лихорадка – тяжелый тип болезни, наблюдаемый в Азии, вызван хантавирусом и передается зараженной полосатой полевой мышью A agrarius mouse.
• Балканская геморрагическая лихорадка, тяжелый тип, встречается в балканских странах, вызван вирусом Добрава, грызун — A flavicollis.
• Легкая и умеренная форма геморрагической лихорадки с синдромом почечной недостаточности вызвана вирусом Сеула и передается зараженными грызунами рода Раттусратута и Rattusnovergicus.
• Умеренная форма геморрагической лихорадки с синдромом почечной недостаточности, наблюдаемая в Европе, вызвана вирусом Puumala и передается грызунами Clethrionomysglariolus.
Вирус обычно попадает к человеку через вдыхание экскрементов зараженных животных (например, мочи, фекалий, слюны). Укус грызуна может также привести к инфицированию человека. На сегодняшний день не существует подтверждения для передачи болезни между людьми.
В группу риска входят лица, связанные с сельскохозяйственной деятельностью, военные (полевые учения), любители походов, дачники и пр.
Диагностика ГЛПС
Проживание в зонах обитания грызунов, вероятность контакта с продуктами их жизнедеятельности (например, уборка дачи после зимы), клиническая картина и лабораторные данные, включая положительный анализ крови на ГЛПС, позволяют поставить окончательный диагноз.
Выполнение биопсии почек не является необходимой мерой.
Анализы при ГЛПС:
• ПЦР-тест;
• ИФА в динамике;
• ОАМ и ОАК;
• проба Зимницкого;
• суточная протеинурия;
• мочевина, креатинин;
• коагулогоамма;
• показатели кислотно-основного состояния;
• электролиты крови и пр.
Инструментальная диагностика проводится по показаниям и включает:
• УЗИ почек;
• ЭКГ;
• ФГДС;
• рентгенографию органов грудной клетки или КТ;
• МРТ и пр.
Симптомы и признаки ГЛПС
Клинические особенности при геморрагической лихорадке с синдромом почечной недостаточности состоят из триады:
• повышение температурной реакции;
• кровоизлияния;
• почечная недостаточность.
К распространенным симптомам на начальном этапе заболевания относят:
• низкое артериальное давление;
• головную боль;
• миалгию и костно-суставные боли;
• озноб;
• жажду;
• абдоминальную и поясничную боль;
• диспепсию.
Инкубационный период – 12-16 дней.
У детей ГЛПС чаще протекает в субклинической форме и при тяжелом течении может осложниться гиповолемическим шоком. Период с момента инфицирования до клинических проявлений – 4-42 дня.
Стадии ГЛПС
Болезнь имеет 5 прогрессирующих стадий:
• инкубационная;
• фебрильная,
• олигоурия;
• полиурия;
• выздоравление.
Только 1/3 пациентов проходит через все стадии.
Фебрильная стадия (лихорадка)
Фебрильная стадия типична для всех пациентов и продолжается 3-7 дней. Болезнь характеризуется резким повышением температуры до 40° C. Пациенты предъявляют жалобы на головную боль, озноб, боль в животе и пояснице, недомогание, снижение остроты зрения.
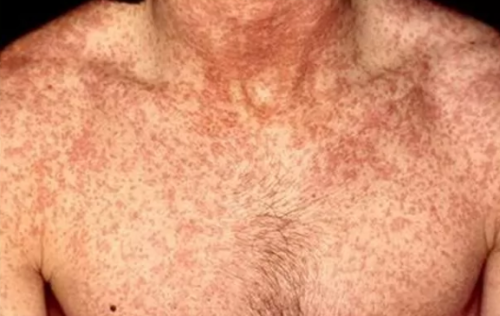
На фоне лихорадки появляется геморрагическая сыпь на грудной клетке, в подмышечных впадинах, шее. На слизистой мягкого неба визуализируются петехии.
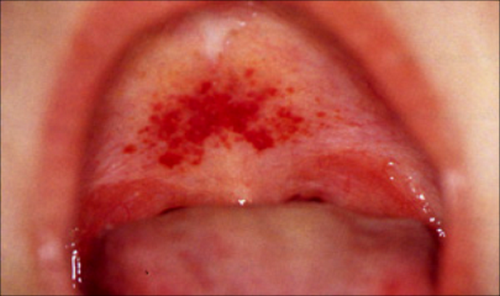
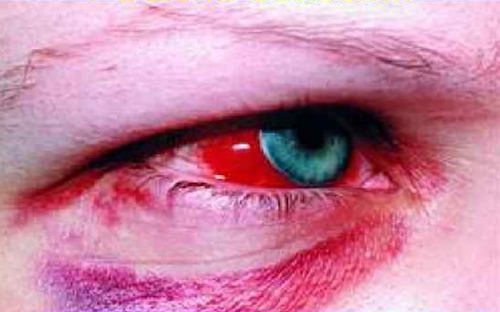
Субконъюнктивальное кровоизлияние отмечено у 30% пациентов. Брадикардия и пастозность лица встречаются достаточно часто. Тахикардия может указывать на предстоящий шок.
С почечной недостаточностью и низким давлением сталкиваются 11% пациентов.
При тяжелом течении осложнением присоединяется острый живот на фоне пареза кишечника. Повышенный уровень амилазы и липазы в сыворотке крови, в сочетании с острой болью в животе, указывает на острый панкреатит. Диагноз можно подтвердить при компьютерной томографии поджелудочной железы, которая показывает отек самого органа и окружающих тканей. У пациентов могут быть судороги или бесцельные движения.
Изменения в анализах:
• повышенный уровень гематокрита, вызванный гемоконцентрацией;
• тромбоцитопения (определяет прогноз и тяжесть почечной недостаточности);
• нормальное количество лейкоцитов или лейкоцитоз с атипичными лимфоцитами;
• нарушения в работе свертывающей системы крови (удлинение времени свертывания и пр.).
В моче временная протеинурия (как правило, разрешается в течение 2 недель) и микрогематурия.
Стадия олигоурии
Олигурическая стадия происходит у 65% пациентов и длится около 3-6 дней.
Для нее характерно острое поражение почек, характеризующееся резким снижением выработки мочи, гипертонией, склонностью к кровотечениям, вызванной уремией, отеками. На этом этапе мочевина и сывороточный креатинин крови достигают наивысшего уровня.
Гипонатриемия, гиперфосфатемия и гиперкалиемия также могут возникать во время олигурической фазы. Серьезное осложнение при неадекватной терапии – отек легких. На данной стадии уровень тромбоцитов возвращается к норме.
Стадия полиурии
Выделение большого количества мочи обычно происходит в течение 2-3 недель. Суточный диурез составляет 3-6 литров, симптомы предыдущих стадий исчезают.
На данном этапе может возникнуть обезвоживание, если инфузионная терапия недостаточна.
Стадия восстановления
Реконвалесценция продолжается до 3-6 месяцев.
Клиническое выздоровление обычно начинается в середине второй недели с постепенным разрешением симптомов и азотемии.
Важно! Концентрационная способность почечных канальцев восстанавливается в течение многих месяцев, поэтому необходимо соблюдать все рекомендации врача и сдавать анализы.
Жалобы пациентов на стадии выздоровления:
• слабость;
• утомляемость;
• мышечные боли;
• снижение аппетита.
Во время выздоровления постепенно восстанавливается привычная масса тела.
Лечение

Терапия зависит от стадии заболевания, уровня дегидратации и состояния гемодинамики. Самый важный шаг в лечении геморрагической лихорадки с почечным синдромом – поддержание гемодинамики пациента и регидратация. Во время активной стадии болезни жизненно необходимо восполнение баланса жидкости и электролитов.
Показания к различным лекарствам основаны на клинике в разные стадии заболевания.
При шоковом состоянии используют препараты, повышающие давление и внутривенно вводят альбумин. Чрезмерная инфузионная терапия может привести к экстравазации, состоянию, когда стенки капилляров начинают пропускать кровь.
Во время олигоурической стадии показаны диуретики (Фуросемид), в случае неэффективности – проведение заместительной почечной терапии, особенно, если есть перегрузка жидкостью, гиперкалиемия и ацидоз.
Если повышено артериальное давление, используют гипотензивные препараты.
Антибиотики показаны только при подозрении на вторичное инфицирование.
При кровотечении переливают кровь и ее компоненты и назначают антагонисты Н 2 –рецепторов.
В случае диссеминированной внутрисосудистой коагуляции вводят свежую плазму или плазмозаменители.
Диета
Рекомендуется питание с низким содержанием натрия и с ограничением жидкости во время олигурической фазы. В период полиурии потребление жидкости свободное.
Из рациона исключают все острые, кислые, копченые, соленые продукты. Пищу готовят с щадящей термической обработкой. Питание – частое, дробное, малыми порциями.
Дальнейшая амбулаторная помощь
Восстановление обычно начинается с 10-11 дня. Период ранней реконвалесценции может продолжаться от нескольких суток до нескольких недель, поэтому необходим тщательный контроль электролитных нарушений и признаков обезвоживания.
Фаза выздоровления длится 3-6 месяцев. Гломерулярные повреждения, как правило, проходят, и концентрационная способность почечных канальцев постепенно улучшается. Последующее наблюдение проводят еженедельно, пока состояние не нормализуется. В последующем анализы контролируют 1 раз в месяц, так как у некоторых пациентов сохраняется протеинурия и повышенное артериальное давление.
У 10-12 % пациентов может развиться пиелонефрит (при присоединении бактериальной флоры), нефросклероз, поэтому наблюдение нефролога обязательно.
Профилактические мероприятия при ГЛПС

Поведение человека может увеличить заболеваемость, поэтому основные превентивные меры включают следующее:
• Правильное хранение пищи и борьба с грызунами.
• Соблюдение мер предосторожности во время проведения садово-полевых работ, в походах, сборах и пр.
• Избегание кемпинга в полях, засаженных зерновыми культурами.
• Хранение соломы вдали от жилища.
Разработка недорогой, безопасной, эффективной и многовалентной вакцины против этой группы вирусов могла бы стать лучшей формой профилактики в эндемичных регионах. Однако высокое генетическое и антигенное разнообразие патогенных хантавирусов в сочетании со спорадическим характером вспышек заболеваний создают серьезные проблемы для разработки эффективных профилактических вакцин.
Осложнения геморрагической лихорадки с почечным синдромом
ГЛПС в редких случаях может привести к развитию следующих состояний:
• забрюшинное кровотечение:
• кровоизлияние в ткани внутренних органов;
• желудочно-кишечное кровотечение;
• отек легких;
• гипопитуитаризм;
• дисфункция гипофиза на фоне атрофии передней доли.
ГЛПС является самоограничивающейся болезнью, и большинство пациентов восстанавливается без осложнений; однако у некоторых людей могут сохраняться симптомы неблагополучия со стороны нервной системы и почек.
Нарушение реабсорбции натрия наблюдается через 12 месяцев после болезни, вызывая его повышенную экскрецию с мочой.
В ряде случаев диагностируют гиперкальциурию и гиперфосфатурию. Приблизительно у 1 из 10 взрослых с терминальной стадией почечной недостаточности в крови присутствуют специфичные к хантавирусу антитела.
В литературе есть данные, что панкреатит и орхит могут быть осложнениями при ГЛПС.
Автор
Виктория Мишина
Дата публикации
07.08.2018
Источник
Геморрагическая лихорадка с почечным синдромом (ГЛПС) – острое вирусное природно- очаговое инфекционное заболевание с нетрансмиссивным механизмом передачи, регистрируемое на территории России в основном в умеренных широтах европейской части и на Дальнем Востоке. Возбудители ГЛПС – вирусы Пуумала, Добрава, Хантаан, Сеул и Амур – относятся к роду Hantavirus, семейства Bunyaviridae. Вирус Пуумала в основном приурочен к лесным ландшафтам европейской части России, наибольшее число случаев ГЛПС регистрируется в Среднем Поволжье и Приуралье (Республика Башкирия, Челябинская, Оренбургская области). Вирус Добрава в последнем десятилетии XX века и в 2000-е годы регистрируется на территории центральных областей России: Рязанской, Тульской, Воронежской, Липецкой, Тамбовской, Курской, а также в Краснодарском крае – в районе Большого Сочи. В европейской части России заболеваемость регистрируется с марта, нарастает в мае-августе, пик приходится на сентябрь-ноябрь, спад – на декабрь-январь. В очагах вируса Добрава выражена осеннее-зимняя сезонность. Очаги вирусов Хантаан, Сеул и Амур находятся в дальневосточных регионах России. Для вируса Амур характерна весенне-летняя или осенне-зимняя сезонность; для вируса Сеул – весенняя, для вируса Хантаан – осенне-зимняя. Источником заражения ГЛПС являются дикие грызуны, механизм передачи вируса – аэрозольный (воздушно-капельный и воздушно-пылевой). Возможен и алиментарный путь заражения через загрязненные продукты питания и воду. Заражение вирусом Пуумала наиболее часто происходит при посещении леса, во время рыбной ловли, при работе на садовом участке, заражение вирусом Добрава – при уходе за домашними сельскохозяйственными животными, работе с фуражом, сеном. Таким образом в очагах вируса Пуумала 6080% заболевших – городские жители, в очагах ГЛПС, вызываемых хантавирусами Добрава, Амур и Хантаан, среди больных преобладают сельские жители. Иммунитет у переболевших сохраняется пожизненно, повторные случаи заболевания ГЛПС, как правило, исключены.
Клиника ГЛПС характеризуется острым началом, цикличностью течения: выделяют начальный период, длящийся 1-3 дня, олигурический период – 4-11-й дни болезни, полиурический период – 12-30-й дни болезни, период реконвалесценции – с 20-30-го дня болезни. Начальный период характеризуется повышением температуры тела, головной болью, миалгиями и артралгиями, жаждой. Могут появиться абдоминальные боли, тошнота, рвота. Часто развивается гиперемия кожи лица, верхней половины туловища, отмечается инъекция сосудов склер. На 3-4-й дни болезни может начаться развитие олигурического периода, характеризующегося уменьшением суточного диуреза, вплоть до анурии и развития острой почечной недостаточности. Геморрагический синдром может проявляться в виде геморрагической сыпи на коже, кровоизлияниях под кожу, носовыми и желудочно-кишечными кровотечениями, гематурией, кровоизлияниями во внутренние органы, субсклеральные гематомы. Могут развиться отек легких и головного мозга, инфекционно-токсический шок. Переход к полиурии связан с улучшением общего состояния больных, в период реконвалесценции при нормализации диуреза в основном сохраняется только астенический синдром. Наряду с тяжелыми и среднетяжелыми формами ГЛПС регистрируются также легкие и стертые формы.
Дифференциальная диагностика
Инфекционные заболевания: лептоспироз, менингококковая инфекция, инфекционный мононуклеоз, клещевой энцефалит и боррелиоз, острые кишечные инфекции;
соматические заболевания: пиелонефрит, панкреатит, почечная колика, заболевания крови, отравления.
Показания к обследованию Лихорадка с общеинтоксикационным синдромом, возникшая у лиц, в последние 1,5 месяца находившихся на территории, эндемичной по ГЛПС, особенно при наличии симптомов: сухость во рту, жажда, нарушение зрения, геморрагические проявления.
Материал для исследований
- Плазма крови – обнаружение РНК вируса;
- сыворотка крови – определение АТ;
- цельная кровь – изоляция вируса.
Этиологическая лабораторная диагностика включает обнаружение специфических АТ IgM и IgG или суммарных АТ к АГ вируса; обнаружение РНК вируса в крови; изоляцию вируса.
Сравнительная характеристика методов лабораторной диагностики
Диагностическая чувствительность выявления РНК вируса методом ПЦР в крови пациентов, взятой на первой неделе заболевания, составляет 85–100%, на второй неделе заболевания – около 40%. При использовании метода ИФА АТ IgM можно определить начиная с 1-го по 7-й, АТ Ig G – со 2-го по 9-й дни болезни, уровень достигает максимальных значений к 8-25-му дню и через 18-22 дня, соответственно. При определении АТ методом ИФА для лабораторного подтверждения ГЛПС необходимо исследовать образцы крови, взятые с интервалом в одну неделю. При использовании метода непрямого МФА (нРИФ) АТ можно определить со 2-3-го дня болезни, к концу второй недели заболевания их уровень достигает пиковых значений. Для подтверждения диагноза ГЛПС с использованием метода МФА также исследуют образцы крови, взятые в динамике: первый – на 2-4-й день болезни, второй – через 2-3 дня; полученные образцы необходимо исследовать одновременно для выявления диагностически значимого нарастания титров АТ к хантавирусам.
Особенности интерпретации результатов лабораторных исследований
Клинический диагноз ГЛПС считают подтвержденным при выделении инфекционного агента, идентифицированного как патогенный для человека вид хантавируса; при выявлении методом ИФА АТ IgM и роста титров IgG в образцах крови, взятых в динамике; при выявлении методом непрямого МФА (РИФ) нарастания титров АТ в образцах крови, взятых в динамике. Обнаружение РНК хантавирусов в крови пациента является основанием для предварительной постановки диагноза.
Источник
Геморрагические лихорадки
Геморрагические лихорадки – это группа острых инфекционных заболеваний, вызванных представителями четырех видов вирусов: аренавирусами, буньявирусами, флавивирусами и филовирусами. Общим для этих заболеваний является тяжелая интоксикация и характерный тромбогеморрагический синдром.
Вирусы, вызывающие геморрагические лихорадки, широко распространены во многих странах мира. Некоторые встречаются и в развитых странах, однако эндемичными районами для большинства видов возбудителей являются Африка, Азия и Южная Америка.
Течение геморрагической лихорадки, в зависимости от возбудителя, может варьироваться от умеренного до крайне тяжелого. Смертность от отдельных вариантов инфекции составляет от 10 до 90 %. Определенные варианты геморрагической лихорадки приводят к тяжелому поражению внутренних органов и нередко к летальному исходу.
Прогноз заболевания зависит от типа вируса, возраста и общего состояния пациента, в частности от активности его иммунной системы.
Синонимы английские
Viral hemorrhagic fevers, hemorrhagicfevers, VHF, VHFs.
Симптомы
Симптомы геморрагических лихорадок различаются в зависимости от типа вируса, вызвавшего заболевание. Общими проявлениями для всех инфекций являются сама сильная лихорадка и повышенная кровоточивость. Симптомы в начальной стадии болезни чаще всего неспецифичны, однако в процессе дальнейшего развития патологического процесса могут появляться признаки поражения определенных органов и систем организма.
Основные симптомы геморрагических лихорадок:
- лихорадка;
- слабость, головокружение;
- мышечные боли;
- гиперемия кожи;
- петехиальная сыпь на коже и слизистых оболочках;
- нарушение сознания;
- покраснение глаз;
- кровь в стуле, рвота с кровью;
- падение артериального давления.
Общая информация о заболевании
Геморрагические лихорадки могут быть вызваны представителями четырех семейств РНК-содержащих вирусов: аренавирусами (Arenaviridae), буньявирусами (Bunyaviridae), филовирусами (Filoviridae) и флавивирусами (Flaviviridae). Аренавирусы вызывают лихорадку Ласса, аргентинскую, бразильскую, венесуэльскую и боливийскую лихорадку, буньявирусы – лихорадку Крым-Конго, лихорадку долины Рифт, геморрагическую лихорадку с почечным синдромом, филовирусы – лихорадку Эбола, флавивирусы – желтую лихорадку, лихорадку Денге и др.
«Резервуарами» вирусов служат некоторые животные и насекомые, чаще всего мелкие грызуны, летучие мыши, москиты, клещи. Как правило, определенные типы геморрагических лихорадок встречаются в основном на территории обитания тех животных, которые являются источником конкретного возбудителя. Например, источник вируса лихорадки долины Рифт, которая распространена на территории Африки, – это москиты. Геморрагическая лихорадка Крым-Конго встречается в Европе, Азии, Африке, ее распространяют клещи. Источник некоторых заболеваний, например лихорадки Эбола, остается неизвестен, предполагают, что им могут быть летучие мыши. Некоторые типы вирусов передаются через кровь или семенную жидкость зараженного животного или человека, через нестерильные иглы. Определенными возбудителями геморрагических лихорадок можно инфицироваться при вдыхании микрочастиц фекалий и мочи животных-переносчиков.
Все представители вирусов, вызывающих геморрагические лихорадки, объединены общим патогенезом. Они склонны поражать эндотелий сосудов, что объясняет развитие геморрагического синдрома при большинстве геморрагических лихорадок. После проникновения вируса в кровь через укусы насекомых, расчесы, ссадины, инъекции, слизистую дыхательных путей сначала формируется локальная реакция на инфекцию, вслед за которой быстро развивается вирусемия и генерализованное поражение системы микроциркуляции (вирус поражает также клетки сосудистой стенки). При проникновении возбудителя в кровь он прилипает к мембране клетки, проникает внутрь нее, активно размножается и распространяется по другим тканям организма. Это сопровождается выделением биологически активных веществ, которые нарушают проницаемость сосудов, реологические свойства крови. Проявлением этого процесса является сыпь, гиперемия кожи, покраснение сосудов склер, могут возникать внутренние кровотечения, сопровождаемые резким падением артериального давления, шоком. Ряд вирусов вызывает поражение костного мозга, в частности мегакариоцитов. Ослабление иммунной системы организма, слабый или запоздалый ответ защитных механизмов может приводить к стремительному развитию патологического процесса, сопровождаемому массивными кровотечениями, полиорганным поражением.
Кто в группе риска?
- Работающие с инфицированными людьми или животными, в частности медицинские работники, биологи, дератизаторы, работники скотоводческих ферм.
- Проживающие в эндемичных районах.
- Употребляющие внутривенные наркотики.
- Те, кто пренебрегает барьерными способами контрацепции.
Диагностика
Диагностика основана на анамнезе, осмотре, результатах лабораторных и инструментальных исследований. При опросе пациента обращается внимание на возможный контакт с возбудителем – путешествие в эндемичные по заболеванию регионы, контакт с животными-переносчиками или инфицированными людьми. Инкубационный период большинства геморрагических лихорадок составляет 10-21 день, поэтому болезнь может развиться уже после возвращения из путешествия в опасный район. При подозрении на наличие геморрагической лихорадки необходимо в условиях стационара в кратчайшие сроки провести ряд исследований, позволяющих дифференцировать болезнь от других заболеваний и установить тип возбудителя:
- Общий анализ крови (без лейкоцитарной формулы и СОЭ). В общем анализе крови при геморрагических лихорадках могут быть выявлены лейкопения и тромбоцитопения. В некоторых случаях, например при лихорадке Ласса, эти изменения отсутствуют. Уровень гемоглобина может понижаться.
- Скорость оседания эритроцитов (СОЭ). Может быть повышена.
- Протромбиновый индекс (ПИ), активированное частичное тромбопластиновое время (АЧТВ) бывают увеличены.
- Фибриноген. Контроль уровня фибриногена и тромбоцитов используется для выявления возможного процесса диссеминированного внутрисосудистого свертывания.
- Анализ используется при подозрении на инфекцию мочевыделительной системы.
- Посев биологических жидкостей: крови, мочи, мазка из зева и носа. Используется для выявления возможных возбудителей инфекции.
- Выявление возбудителя инфекции в крови методом полимеразной цепной реакции (ПЦР).
- Выявление в крови антител к возбудителю инфекции.
Все диагностические манипуляции следует выполнять с особой осторожностью в связи с высокой болезнетворностью возбудителей.
Лечение
Лечение данной группы заболеваний должно проводиться в условиях стационара. Специфическая терапия большинства возбудителей геморрагических лихорадок отсутствует. Лечебная тактика определяется состоянием пациента и направлена на поддержание жизненных функций и предотвращение возможных осложнений. Такие противовирусные препараты, как рибавирин, могут снизить активность возбудителя.
Профилактика
- Контроль популяции мелких грызунов;
- использование средств индивидуальной защиты против укусов москитов, клещей;
- своевременная вакцинация против определенных видов геморрагических лихорадок, например желтой лихорадки, перед посещением эндемичных районов;
- соблюдение гигиенических правил.
Рекомендуемые анализы
- Общий анализ крови
- Общий анализ мочи с микроскопией осадка
- Скорость оседания эритроцитов (СОЭ)
- Коагулограмма № 1 (протромбин (по Квику), МНО)
- Активированное частичное тромбопластиновое время (АЧТВ)
- Фибриноген
Источник
